트랜스페린
| 트랜스페린 | |||||||||
|---|---|---|---|---|---|---|---|---|---|
| 식별자 | |||||||||
| 상징 | Transferrin | ||||||||
| Pfam | PF00405 | ||||||||
| InterPro | IPR001156 | ||||||||
| PROSITE | PDOC00182 | ||||||||
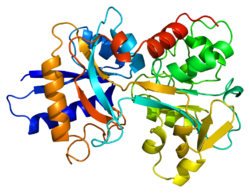
| SCOP | 1lcf | ||||||||
| SUPERFAMILY | 1lcf | ||||||||
| |||||||||
트랜스페린(영어: transferrin)은 척추동물에서 발견되는 당단백질로 혈장에서 철(Fe)에 결합하여 철의 운반을 매개한다.[5] 간에서 생산되며 두 개의 Fe3+ 이온과 결합할 수 있는 부위를 가지고 있다.[6] 사람 트랜스페린은 TF 유전자에 의해 암호화되어 있으며 분자량은 76kDa이다.[7][8]
트랜스페린 당단백질은 철과 강하게 결합하지만 그 결합은 가역적이다. 트랜스페린과 결합한 상태인 철은 체내 존재하는 전체 철의 0.1%보다 적지만(4mg), 교체 속도가 가장 빠르며(25mg/24h) 체내에 가장 중요한 철의 저장고 역할을 한다. 철과 결합하는 친화도는 매우 높으며, pH 7.4에서 결합상수는 1020 M−1이다.[9] 그러나 pH가 중성 이하로 떨어지면 친화도가 계속 떨어진다.[10] 트랜스페린은 척추동물의 다양한 체액에 들어 있다.[11][12] 몇몇 척추동물은 혈림프에 트랜스페린과 유사하게 작용하는 단백질이 존재한다.[11][13]
철과 결합하지 않은 트랜스페린은 아포트랜스페린(apotransferrin)이라고 한다.
같이 보기[편집]
각주[편집]
- ↑ 가 나 다 GRCh38: Ensembl release 89: ENSG00000091513 - 앙상블, May 2017
- ↑ 가 나 다 GRCm38: Ensembl release 89: ENSMUSG00000032554 - 앙상블, May 2017
- ↑ “Human PubMed Reference:”. 《National Center for Biotechnology Information, U.S. National Library of Medicine》.
- ↑ “Mouse PubMed Reference:”. 《National Center for Biotechnology Information, U.S. National Library of Medicine》.
- ↑ Crichton RR, Charloteaux-Wauters M (May 1987). “Iron transport and storage”. 《European Journal of Biochemistry》 164 (3): 485–506. doi:10.1111/j.1432-1033.1987.tb11155.x. PMID 3032619.
- ↑ Hall DR, Hadden JM, Leonard GA, Bailey S, Neu M, Winn M, Lindley PF (January 2002). “The crystal and molecular structures of diferric porcine and rabbit serum transferrins at resolutions of 2.15 and 2.60 A, respectively”. 《Acta Crystallographica. Section D, Biological Crystallography》 58 (Pt 1): 70–80. doi:10.1107/s0907444901017309. PMID 11752780.
- ↑ Yang F, Lum JB, McGill JR, Moore CM, Naylor SL, van Bragt PH, 외. (May 1984). “Human transferrin: cDNA characterization and chromosomal localization”. 《Proceedings of the National Academy of Sciences of the United States of America》 81 (9): 2752–6. Bibcode:1984PNAS...81.2752Y. doi:10.1073/pnas.81.9.2752. PMC 345148. PMID 6585826.
- ↑ Kawabata H (March 2019). “Transferrin and transferrin receptors update”. 《Free Radical Biology & Medicine》 133: 46–54. doi:10.1016/j.freeradbiomed.2018.06.037. PMID 29969719. S2CID 49674402.
- ↑ Aisen P, Leibman A, Zweier J (March 1978). “Stoichiometric and site characteristics of the binding of iron to human transferrin”. 《The Journal of Biological Chemistry》 253 (6): 1930–7. doi:10.1016/S0021-9258(19)62337-9. PMID 204636.
- ↑ Nicotra S, Sorio D, Filippi G, De Gioia L, Paterlini V, De Palo EF, 외. (November 2017). “Terbium chelation, a specific fluorescent tagging of human transferrin. Optimization of conditions in view of its application to the HPLC analysis of carbohydrate-deficient transferrin (CDT)”. 《Analytical and Bioanalytical Chemistry》 409 (28): 6605–6612. doi:10.1007/s00216-017-0616-z. PMID 28971232. S2CID 13929228.
- ↑ 가 나 MacGillivray RT, Moore SA, Chen J, Anderson BF, Baker H, Luo Y, 외. (June 1998). “Two high-resolution crystal structures of the recombinant N-lobe of human transferrin reveal a structural change implicated in iron release”. 《Biochemistry》 37 (22): 7919–28. doi:10.1021/bi980355j. PMID 9609685.
- ↑ Dewan JC, Mikami B, Hirose M, Sacchettini JC (November 1993). “Structural evidence for a pH-sensitive dilysine trigger in the hen ovotransferrin N-lobe: implications for transferrin iron release”. 《Biochemistry》 32 (45): 11963–8. doi:10.1021/bi00096a004. PMID 8218271.
- ↑ Baker EN, Lindley PF (August 1992). “New perspectives on the structure and function of transferrins”. 《Journal of Inorganic Biochemistry》 47 (3–4): 147–60. doi:10.1016/0162-0134(92)84061-q. PMID 1431877.