질소염기
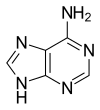


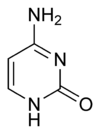

질소염기(窒素塩基, 영어: nitrogenous base)는 염기의 화학적 특성을 가지고 있고, 질소 원자를 지니고 있는 유기 화합물이다. 질소염기의 주요 생물학적 기능은 핵산에서 유전 정보를 저장, 전달하는 것이다. 질소염기는 질소 원자의 비공유 전자쌍에 기본적인 특성을 지니고 있다.
질소염기는 일반적으로 두 가지 모체 화합물인 피리미딘과 퓨린의 유도체로 분류된다.[1] 질소 염기는 무극성이며, 방향족성 때문에 평면 구조를 가지고 있다. 피리미딘과 퓨린은 둘 다 피리딘과 유사하므로 약한 염기이며, 친전자성 방향족 치환에 상대적으로 반응하지 않는다.[2]
핵산에서의 역할[편집]
생물학에서 질소염기는 핵산에서의 역할 때문에 점차적으로 핵염기로 불리고 있는 추세이다. 질소염기의 평면 구조는 DNA와 RNA의 구성 요소로서의 역할을 고려할 때 특히 더 중요하다. 5가지 질소 염기가 뉴클레오타이드의 구성에 사용되며, 이는 DNA 및 RNA와 같은 핵산을 생성하는 데 쓰인다. 핵산을 구성하는 데 사용되는 질소염기에는 아데닌(A), 구아닌(G), 사이토신(C), 티민(T), 유라실(U)이 있다. 티민과 유라실은 6원자 헤테로고리의 5번 탄소(C5)에 메틸기가 존재하거나 존재하지 않는 것으로 구별된다.[3] 질소염기는 DNA 두 가닥 사이에 수소 결합을 형성하여 DNA 이중 나선을 이루도록하거나 뉴클레오타이드에서 발견되는 생물학적 촉매로 기능하게 한다. 아데닌은 항상 티민과 염기쌍을 형성하고, 구아닌은 항상 사이토신과 염기쌍을 형성한다. 이들은 상보적인 염기쌍을 형성하고 염기들은 수소 결합으로 연결되어 있다. DNA에서 아데닌은 티민과 2개의 수소 결합을 형성하고, RNA에서 아데닌은 유라실과 2개의 수소 결합을 형성하며, 구아닌은 사이토신과 3개의 수소 결합을 형성한다. 이들 분자 구조의 다양성으로 인해 자연에서 생성되는 다양한 비정규 염기쌍들이 존재한다.[3] 유라실은 RNA에만 존재하며, 티민을 대신한다. 피리미딘 계열 염기에는 티민, 사이토신, 유라실이 있으며, 이들은 단일 고리 구조를 가지고 있다. 퓨린 계열 염기에는 아데닌, 구아닌이 있으며, 이들은 2개의 고리 구조를 가지고 있다.[4]
같이 보기[편집]
각주[편집]
- ↑ Nelson, David L. and Michael M Cox (2008). Lehninger Principles of Biochemistry, ed. 5, W.H. Freeman and Company. p. 272. ISBN 071677108X.
- ↑ Carey, Francis A. (2009). Organic Chemistry, ed. 6, Mc Graw Hill. p. 1206. ISBN 0072828374.
- ↑ 가 나 Soukup, Garrett A. (2003), 〈Nucleic Acids: General Properties〉, 《eLS》 (영어), American Cancer Society, doi:10.1038/npg.els.0001335, ISBN 9780470015902
- ↑ Angstadt, Carol N (1997) Purine and Pyrimidine Metabolism. library.med.utah.edu
