유도만능줄기세포
유도만능줄기세포(誘導萬能 - 細胞, 영어: induced pluripotent stem cell, iPS cell/iPSC) 또는 역분화 줄기세포는 다능성이 없는 성인의 피부세포와 같은 체세포에 역분화를 일으키는 4가지 특정 유전자를 도입한 후 발현시키거나 역분화를 일으키는 4가지 유전자가 도입된 세포에서 만들어진 역분화 유도 단백질을 추출하여 이를 다시 체세포에 주입함으로써 배아 줄기세포와 같은 다능성을 갖는 줄기세포를 만들 수 있는데 이를 유도 만능 줄기세포 또는 역분화 줄기세포라고 한다.
2006년 일본 교토대 야마나카 신야 교수팀은 생쥐의 피부 섬유아세포에 몇 가지 유전자를 도입하여 배아줄기세포처럼 만능성을 가진 줄기세포를 만드는데 성공했다. 이듬해인 2007년에 야마나카 교수팀은 성인의 피부세포에 유전자를 도입하여 유도만능줄기세포를 만드는데 성공하였다. 이미 성숙하고 분화된 세포를 미성숙한 세포로 역분화시켜서 다시 모든 조직으로 발전시킬 수 있다는 사실을 발견하고 증명한 공로가 인정되어, 야마나카 신야 교수는 존 거든 교수와 함께 하며 2012년 노벨 생리학·의학상 수상자로 선정되었다.[1]
만능성의 개념[편집]
정상 발달 과정을 거치면서 세포들은 처음의 분화되지 않은 상태에서 점차적으로 분화되어 기능이 전문화된 상태로 변화한다. 수정란의 세포들은 전능(totipotent)한데, 이는 그 세포들이 태반과 같은 배아 이외의 구조 비롯하여 모든 종류의 조직들로 발생할 수 있다는 것을 의미한다. 발달 단계가 진행되면서 배반포가 되면, 내부세포괴(inner cell mass)와 바깥쪽 세포들로 구분 할 수 있는데, 이 때 안쪽의 세포들은 모든 종류의 배아 체세포와 생식세포로 발생할 수 있는 만능성(pluripotent)을 가진다.
유도만능줄기세포의 장점[편집]
배반포의 내부세포괴에서 추출한 배아줄기세포는 만능성을 가지고 내배엽, 중배엽, 외배엽 세포로 모두 분화가 가능한 세포이다. 인간 배아줄기세포는 파킨슨병, 척수손상, 당뇨 등의 질병을 치료하는 데에 이용될 수 있다고 알려져 있다. 그러나 배아줄기세포는 배아를 파괴한다는 윤리적 문제와 환자의 몸 속에 이식하였을 때 거부반응이 일어날 수 있다는 한계가 존재하였다. 그러나 유도만능줄기세포는 수정란에서 발생하고 있는 배아를 파괴해야만 줄기세포를 얻을 수 있는 기존 배아줄기세포 연구의 윤리적인 문제를 한 번에 해결했다는 점에서 큰 의미를 갖는다. 또한 환자의 체세포를 줄기세포로 전환시키므로 면역 거부 반응 문제가 없다.
유도만능줄기세포의 유도방법[편집]
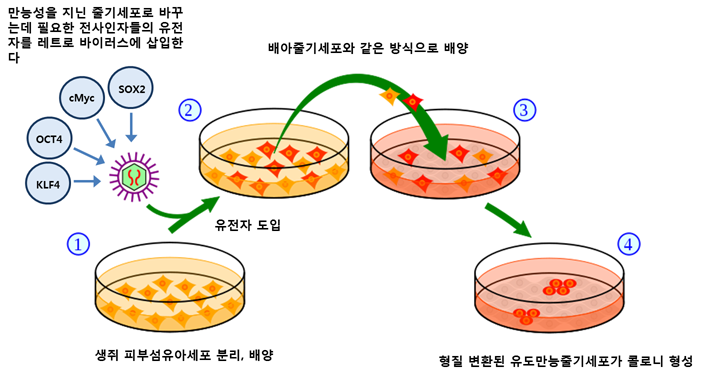
일본 교토대 야마나카 신야 교수팀은 레트로바이러스(retrovirus)를 이용하여 생쥐의 피부 섬유아세포에 Oct3/4, Sox2, c-Myc, Klf4 유전자를 도입시켜 유도만능줄기세포를 만들었다. 야마나카 신야 교수는 이 4가지 유전자만 도입해도 체세포에 만능성을 충분히 유도할 수 있는 것을 밝혔다.[2]
먼저, 야마나카 교수는 난모세포에 체세포 핵이식을 했을 때 또는 체세포와 배아줄기세포를 융합시켰을 때 세포에 만능성이 유도된다는 것에 기초하여, 배아줄기세포 안에서 만능성을 유지하게 하는데 중요한 역할을 하는 유전자들은 분명 체세포에 만능성을 유도하는 데에 중요한 역할을 할 것이라는 가설을 세웠다. 그리고 배아줄기세포 안에서 만능성을 유지하게 하는데 중요한 역할을 하는 여러 가지 유전자들 중 24개의 유전자(Ecat1, Dpp5(Esg1), Fbx015, Nanog, ERas, Dnmt3l, Ecat8, Gdf3, Sox15, Dppa4, Dppa2, Fthl17, Sall4, Oct4, Sox2, Rex1, Utf1, Tcl1, Dppa3, Klf4, b-cat, cMyc, Stat3, Grb2)를, 체세포에 만능성을 유도할 것이라고 생각되는 후보로 선별하였다.
레트로바이러스로 24개의 유전자를 도입시키기 전, 생쥐의 피부 섬유아세포의 Fbx15 프로모터 옆에 neomycin/lacZ 유전자를 상동재조합으로 삽입한다. Fbx15는 만능성을 가진 줄기세포에서 활성화되는 프로모터로써 neomycin/lacZ 유전자를 발현하는 유전자는 G418(단백질합성의 저해에 의해 강력한 세포독성을 나타내는 아미노배당체계 항생물질의 하나)[3]에 저항성을 가진다. 그 다음, 레트로 바이러스를 이용하여 24개의 유전자 모두를 이 생쥐 피부 섬유아세포들에 형질도입 시켰다. 이 세포들을 G418이 0.3mg/ml정도 있는 STO 지지세포 위에서 배양한다. 유전자가 도입된 세포 중 일부 세포가 유도만능줄기세포가 되어 콜로니가 형성된다.
24개의 유전자 중 체세포에 만능성을 유도하는 중요한 요인들을 알아내기 위해, 24개의 유전자 중 하나씩을 없애가면서 생쥐 피부 섬유아세포에 유전자를 유도한다. 24개의 유전자 중에서 하나의 유전자가 없어지는 영향으로 유도만능줄기세포가 되어 콜로니가 형성되는 정도가 변하는 것을 측정하는 과정을 통하여, 생쥐 피부섬유아세포를 만능성을 지닌 줄기세포로 바꾸는 데 충분한 네 개의 전사인자(Oct3/4, Sox2, c-Myc, Klf4)를 찾았다. 이로써 야마나카 교수는 네 개의 전사인자를 사용하여 유도만능줄기세포를 만드는 데 성공하였다. 유도만능줄기세포는 배아줄기세포와 비슷한 성질을 나타낸다는 것을 볼 수 있다. 배아줄기세포와 유도만능줄기세포는 형태, 발현되는 유전자(RT-PCR, DNA 마이크로어레이를 통해 비교), DNA메틸화(바이설파이트 게놈서열분석을 통해 비교)패턴이 비슷하다.
2006년, 생쥐 섬유아세포에 네 개의 전사인자를 도입하여 유도만능줄기세포를 만드는 데 성공한 야마나카 교수는, 이듬해에 인간 피부 섬유아세포에도 같은 네 개의 전사인자를 유도 시켜 인간 유도만능줄기세포를 만드는 것도 성공하였다.[4] 같은 해에 미국 위스콘신 메디슨 대학 제임스 톰슨 교수팀은 레트로바이러스로 유전자(Oct4, Sox2, Nanog and Lin28)를 도입하여 인간의 피부세포로부터 유도만능줄기세포를 만드는데 성공하였다.[5]
유도 세부 과정[편집]
생쥐의 섬유아세포가 유도만능줄기세포로 진행되는 과정은 유전자들이 순차적으로 활성화되는 일련의 단계를 거친다.
- alkaline phosphatase(AP) → stage-specific embryonic antigen 1 (SSEA1) → endogenous Nanog 와 Oct4 유전자
이 중 AP는 네 가지 유전자(Oct4, Sox2, Klf4, c-Myc)를 세포 내에 발현시킨 뒤 3일부터 발현되기 시작하고, SSEA1 은 9일부터, 그리고 Oct4 와 Nanog는 16일부터 발현되기 시작해 유도만능줄기세포로 변화되게 된다. 따라서 12-16일간 동안은 4가지 유전자의 계속적인 발현이 있어야 완전한 유도만능줄기세포를 형성할 수 있다. [6]
관련 역분화 인자[편집]
Sox2[편집]
SOX2 유전자는 만능성을 유지하는데 결정적 역할을 한다. SOX2는 윈트 신호전달 경로를 억제하는 또 다른 유전자 'DKK1'의 발현을 좌우함으로써 결과적으로 성체줄기세포의 '다분화능(multipotent)'을 유지할 뿐 아니라 특정 세포로의 분화 과정도 조절한다. 이 같은 'SOX2-DKK1-윈트신호' 체계에 따른 SOX2 유전자의 작용 원리는 성체줄기세포뿐 아니라 배아줄기세포나 유도만능 줄기세포에서도 같다. [7]
c-Myc[편집]
c-Myc 유전자는 세포 증식과 형질전환을 촉진시키는 역할을 한다. 또한 히스톤아세틸전달효소와 관계하여 히스톤을 아세틸화 시켜서 DNA와의 접촉이 느슨하게 함으로써 유전자의 전사억제상태를 완화시킨다. 이를 통해 Oct3/4와 Sox2가 특정한 유전자 위치에 잘 결합하여 전사를 유도할 수 있도록 한다.[8] 그러나 이 유전자는 암 유전자의 일종으로 야마나카 교수가 뒷날 세포를 초기화시키는데 필수적이지 않다는 사실을 밝혀냈다.
Klf4[편집]
Klf4는 p53을 직접 억제하는 것으로 알려졌다.[9] p53은 배아줄기세포의 분화과정에서 Nanog를 억제하는 것으로 알려져있다.[10] 유도만능줄기세포는 p53 단백질의 발현이 섬유아세포보다 적다. 그러므로 Klf4는 p53을 억제시키므로써 Nanog를 활성화시키고 배아줄기세포에서 특별히 발현되는 유전자를 활성화 시킬 것이다.[11]
Oct-3/4[편집]
Oct-3/4(octamer-binding transcription) 또는 POU5F1 (POU domain, class 5, transcription factor 1)로 알려진 이 전사 인자는 신체에서 POU5F1 유전자에 의해서 암호화된 단백질이다. Oct-3/4는 POU 가계의 호메오 도메인 전사인자이다. 이 단백질은 미분화 된 배아줄기세포의 자가재생에서 중요하게 관련되어있다. 이와 같이, 이 전사인자는 미분화 세포에 대한 마커로서 사용된다. Oct-3/4의 발현은 꼭 통제되어야한다. 너무 많이 혹은 너무 적게 Oct-3/4가 발현되면 미분화 세포가 분화되는 원인이 된다.
안전한 유도만능줄기세포 생산방법[편집]
초기에 유도만능줄기세포를 생산한 방법은 바이러스를 이용하여 주입한 역분화 인자의 과발현을 유도하여 역분화가 일어나게 하여 만능성을 얻게 하는 것이다. 그러나, 역분화 인자 주입에 바이러스를 이용할 경우 바이러스에서 유래된 유전자가 세포에 같이 삽입되어 유전자의 변화를 일으키거나 다른 위험이 발생될 수 있다. 따라서 유전자 내 외래유전자 삽입이 없는 단백질이나 플라스미드를 이용한 역분화 방법이 개발되었다.
형질주입된 플라스미드를 세포 내의 핵에 삽입하기 위해서 또 다른 나노캐리어인 Xfect라고 불리는 나노입자(nanoparticle)을 사용한다. 이 방법을 통해서는 유도만능줄기세포주를 수립할 수 있다.
또한 프로그램을 개작할 수 있는(reprogrammable) 생쥐를 이용하여 체내서 유발된 테라토마에서 유도만능줄기세포를 생산하는 기술이 있다. 이 방법은 역분화 인자 유전자들의 발현이 독시사이클린에 의해 조절되는 세포로부터 만들어진 생쥐를 이용한다. 이렇게 수립된 유도만능줄기세포는 기존의 유도만능줄기세포보다 분화 능력이 뛰어나다고 분석되고있다. 기존의 방법은 피부세포 1000개에 역분화를 시도하였을 때 그 중 1개가 역분화줄기세포로 되는 매우 낮은 역분화 효율을 나타냈다.
유도만능줄기세포의 적용[편집]
역분화 기술의 발전[편집]
초기에는 체세포에 유전자를 도입시킬 때 레트로바이러스 벡터를 사용했다. 레트로바이러스 벡터를 사용하기 때문에 도입시킨 유전자들이 게놈에 무작위로 삽입되어 암을 유발하는 부작용이 있었다. 2008년 야마나카 신야 교수팀은 바이러스 벡터 없이 Oct3/4, Sox2, c-Myc, Klf4를 포함하는 cDNA를 쥐의 체세포에 삽입하여 테라토마 등의 부작용이 없는 유도만능줄기세포를유도하였다.[12] 또한 최근에는 바이러스 시스템 대안으로 저분자 화합물, 단백질, 비바이러스성 비삽입성 벡터(에피솜 벡터) 등을 이용하여, 만능성을 유지하게 하는 유전자들이 체세포의 게놈에 통합되지 않고도 세포 내로 전달될 수 있게 하는 방법을 사용하고 있다. 이러한 역분화 기술들이 개발되고 있으나 바이러스 이용 기법에 비해 현저히 낮은 역분화 효율 문제와 재현성 확보 문제가 지속적으로 제시되고 있다.
체세포가 유도만능줄기세포가 되도록 유도할 때 발암유전자를 포함하는 인자(c-Myc,Klf4)를 레트로 바이러스를 이용하여 도입하기 때문에 암 유발 및 세포기능 변화 가능성이 있다는 위험이 있었다. 하지만 2008년 야마나카 신야 교수팀은 Myc 유전자 없이도 유도만능줄기세포를 만들 수 있는 방법을 개발하였다.[13] 이후 역분화를 유도하는 원로세포를 피부세포가 아닌 내재적으로 Sox2, Myc, Klf4를 발현하고 있는 성체줄기세포인 신경줄기세포를 사용하여 나머지 3개의 인자중 다른 발암유전자인 Klf4도 없이 역분화 줄기세포를 제작하였고 이후 피부세포에서도 C-Myc, Klf4를 발현하고 있어서 후속 연구에서 Oct4와 Sox2만으로도 역분화에 성공한 보고가 있다. 이로써 발암유전자를 사용하지 않고 유도만능줄기세포를 만드는 것이 가능하게 되었다.
특정한 종류의 세포들의 만능성을 유도하는 데 있어서, 네 가지 요인(Oct3/4, Sox2, c-Myc, Klf4)보다 더 적은 요인만 있어도 가능하다는 것이 밝혀졌다. 예를 들어, 쥐의 신경 줄기세포를 유도할 경우 오직 Oct4만이 필요하다. 유승권 고려대학교 생명공학부 교수팀은 'Id3' 유전자를 쥐의 체세포에 넣어 일단 신경줄기세포를 만든 뒤, 이를 'Oct4' 유전자만 사용해 만능줄기세포로 유도하였다.[14]
향후 다양한 시장수요에 맞는 품질의 유도만능줄기세포를 만들어내고 그 상용화시기를 앞당기기 위해서는, 먼저 임상적으로 안전하면서 효율이 높은 역분화 기술을 개발하는 것이 필수적으로 선행돼야 한다.
이후 2010년 세계 최초로 배아줄기세포에서 추출한 단백질을 체세포에 주입해 iPS를 만드는 데 성공한 서울대병원 김효수 교수와 의생명연구원 권유욱 교수팀이 2015년 생물재료학 분야의 국제 학술지인 '바이오머티리얼스' 5월호에 실은 논문에는 배아줄기세포가 아닌 iPS에서 추출한 단백질을 체세포에 주입할 경우 역분화 과정의 효율을 크게 향상시킬 수 있다고 한다. 김 교수와의 인터뷰에서 김교수는 "배아줄기세포의 단백질을 주입했을 때보다 iPS에서 추출한 단백질을 주입한 체세포는 iPS로 역분화하는 속도가 10배 이상 빨랐다"고 말했다. 김 교수팀은 이런 효과를 낳는 물질이 iPS 단백질 중 '지스캔4'(Zscan4)란 것도 밝혀냈다. 김 교수는 "이 단백질이 체세포를 젊게 만드는 작용을 하면서 체세포의 리프로그래밍이 훨씬 더 효율적으로 이뤄지도록 했다"고 말했다. 리프로그래밍이란 특정 세포가 어떤 세포로 분화할지 하는 운명을 결정하는 프로그램을 다시 바꾸는 것을 가리킨다.
체세포를 역분화 시키는 것이아닌 성체줄기세포인 신경줄기세포에 역분화를 유도하는 방법이 있다. 이러한 방법을 이용하면 일반적인 체세포인 피부세포가 1000개에 역분화를 유도시켰을 때 그중 1개가 역분화줄기세포가 되는 것과 같이 굉장히 낮은 효율을 보여주는데 성체줄기세포인 신경줄기세포를 역분화를 유도시키면 체세포보다 약 100배에서 3000배 높은 역분화 효율을 나타내었다. 또한 역분화 시간도 체세포의 역분화 시간인 2주에 비해 약 5배 빠른 역분화를 보여주며 높은 효율을 나타냈다. 결론적으로 역분화 유도에 내부적으로 역분화 인자를 발현하는 세포인 성체줄기세포를 사용하면 외부적으로 그 인자를 처리해 주어도 역분화를 유도할 수 있다는 것이다.
줄기세포치료제로써의 유도만능줄기세포[깨진 링크(과거 내용 찾기)][편집]
유도만능줄기세포를 포함한 줄기세포들은 파킨슨병이나 제1형 당뇨병과 같은 질병으로 인해 손상된 세포들을 대체할 수 있다. 유도만능줄기세포를 이용한 줄기세포치료는 자가이식이 가능하므로 환자가 면역 거부 반응을 일으킬 확률을 낮춘다. 하지만 돌연변이나 다른 유전적인 이상을 일으킬 수도 있다는 문제점들이 있다. 따라서 환자들에게 안전하게 사용되기 위해서 많은 후속 연구가 필요하다.
의학적 연구에 사용[편집]
iPS 세포의 생산과제는 위에서 언급한 문제 때문에 계속 연구해야 할 주요 절충안은 유전공학적인 장벽에 의존하지 않는 대부분의 방법은 비효율적인 반면, 트랜스젠의 통합에 의존하는 방법들은 방대한 기술과 방법이 시도되었지만 불완전한 재프로그래밍과 종양 발생의 문제에 직면하고 있는 실정이다. 또 다른 대규모 전략들은 iPS 세포의 단백질 특성화를 수행하는 것이다. 추가 연구와 새로운 전략은 최적의 해결책을 제시해야 한다. 한 가지 접근방식은 이러한 전략의 긍정적인 측면을 활용하여 iPS 세포에 대한 세포 재프로그래밍을 위한 효과적인 기법으로 결합하려고 시도할 수 있다.
또 다른 접근법은 질환표현형을 구현할 수 있는 치료용 약물을 식별하기 위해 환자로부터 파생된 iPS 세포를 사용하는 것이다. 예를 들어, p63 유전자가 변이되는 EEC(Ectoderal Edysplasia Syndrome)의 영향을 받는 환자로부터 파생된 iPS 세포는 리프로그래밍 요인(OSKM)에 의해 리프로그래밍 되어 역분화줄기세포로 되고, 이를 분화시켜 환자 특이적 맞춤형 세포치료제를 개발할 수 있는데에 의의가 있다.
질환표현형에 적합
체세포를 얻어 유도만능줄기세포를 만들어서 체외에서 분화시킴으로써 여러 가지 질병의 경과를 연구하여 질병 모델을 얻을 수 있다. 현재 다양한 질병에 걸린 환자들로부터 유도만능줄기세포가 만들어져 연구되고 있으며, 이러한 질병 모델들에게서 질환과 관계된 표현형들이 관찰되고 있다. 예를 들어 척수근위축증 환자의 유도만능줄기세포들의 경우, 점진적으로 운동 뉴런이 소실되는 것이 관찰되었다. 알파1-안티트립신-결핍증 환자의 유도만능줄기세포를 간세포로 분화된 이후에 관찰한 결과 지질과 글리코겐의 축적 정도가 증가하였다. 알츠하이머병의 질병모델링에도 유도만능줄기세포가 사용된다.
신약 개발에서의 세포 기반 연구[편집]
유도만능줄기세포들에 기초하여 생체 외에서 분화된 세포들은 신약의 개발과 신약의 안전성 검사에 많이 이용한다. 예를 들어 키네틴의 경우 가족성자율신경실조증의 원인이 되는 IKBKAP 유전자의 비정상적인 이어 맞추기를 부분적으로 정상화한다는 것이 밝혀졌다.[15] 또한 QT 연장증후군에서 베타차단제와 이온채널차단제 역시 표현형을 조절하는 데 효과적이라고 밝혀졌다.[16]
불임치료[편집]
2009년 7월 8일, 영국 뉴캐슬 대학과 뉴잉글랜드 복잡계 연구소(NESCI)의 카림 나예니아 박사 연구팀은 인간 배아줄기세포에서 세계 최초로 시험관 정자를 생산했다. 배아줄기세포는 어떤 종류의 세포로도 분화할 수 있지만 정자로 성장시키는 데 성공한 것은 이들이 처음이다. 그러나 유도만능줄기세포를 이용한 것은 아니다. 이란 출신 카림 나예니아 박사는 독일에서 연구하다가, 독일 정부가 인간 배아줄기세포 연구를 금지시키자, 2006년 영국 뉴캐슬 대학으로 이주해 연구를 계속했다.[17]
2011년 8월 5일, 일본 교토대 사이토 미치노리(齊藤通紀) 교수 연구팀은 세계 최초로 쥐의 체세포를 조작해 유도만능줄기세포로 만들고 다시 조작해 정자를 만들어 체외에서 수정해 새끼 쥐를 출산시키는데 성공했다. 같은 날 셀 지 인터넷판에도 소개되었다. 쥐의 배아줄기세포에서 정자를 만든 것도, 쥐의 유도만능줄기세포에서 정자```를 만든 것도, 정자를 통해 수정 및 출산에 성공한 것도 세계 최초다.[18]
2012년 미국 피츠버그 대학 연구팀이 생식기능이 정상인 남성의 피부세포를 유도만능줄기세포로 환원시켜, 정자전구세포를 만드는데 세계최초로 성공했다.
2014년 5월 1일, 미국 스탠퍼드 대학 줄기세포생물학·재생의학연구소의 레이호 페라 박사는 Y염색체 이상으로 정자가 없는 무정자증 남성의 피부세포를 유도만능줄기세포로 환원시켜 이를 쥐의 고환에 주입, 초기단계의 정자세포인 정자전구세포로 자라게 하는 데 성공했다. 세계최초로 무정자증 남성의 피부로 정자를 만들었다.[19]
한계
2006년, Yamanaka 연구팀은 체세포에서 pluripotency를 유도할 수 있는 24개의 gene을 후보군으로 선정하였다. 이중 Oct3/4 와 Sox2가 유도만능줄기세포의 생성에 필수 인자임을 밝히고, 이전 연구들에서 pluripotency를 유지하는 핵심 전사 인자 중 하나로 알려졌던 Nanog는 실제 리프로그래밍 기전에는 관련이 없다고 보고하였다. 또한 c-Myc 과 Klf4 여시 유도만능줄기세포의 생성에 중요한 역할을 한다는 것을 밝혀냈고, 이 두가지의 종양 관련 인자들은 다른 암유전자들은 다른 암유전자들(E-Ras, Tcl1, ß-catenin, Stat3)로는 대체 불가능하다고 보고하였다. 이후 2007년, Thomson 연구팀은 Yamanaka 연구팀의 실험과 다른 조합(Oct4, Sox2, Nanog, Lin28)을 이용하여 실험을 실행하였는데, 그 결과 기존의 연구에서 리프로그래밍 기전에 관련이 없는 것으로 알려졌던 Nanog 인자가 리프로그래밍의 효율을 높이며 리프로그래밍 된 세포의 초기 생존률을 높이는데 기여하는 것을 밝혔으며, Lin28 역시 유도만능줄기세포의 생성에 관여한다고 보고하였다. 여러 연구에서 유도만능줄기세포의 기본 메커니즘을 분석하고, 기술의 완성도를 높이기 위한 시도들이 이뤄졌지만 유도만능줄기세포는 아직 임상적 적용에 있어 몇 가지 한계점을 가지고 있다. 유전자 도입에 바이러스를 이용한다는 점(integrated iPSCs)과 c-Myc, Klf4 등의 인자가 가지는 tumorigenicity는 유도만능줄기세포의 대표적인 한계점으로 꼽힌다.[20]
각주[편집]
- ↑ http://www.nobelprize.org/nobel_prizes/medicine/laureates/2012/#
- ↑ Takahashi K, Yamanaka S(2006). Induction of pluripotent stem cells from mouse embryonic and adult fibroblast cultures by defined factors. Cell 126: 663-676
- ↑ https://terms.naver.com/entry.nhn?cid=561&docId=435663&mobile&categoryId=561
- ↑ Takahashi K, Tanabe K, Ohnuki M, Narita M, Ichisaka T, Tomoda K et al (2007). Induction of pluripotent stem cells from adult human fibroblasts by defined factors. Cell 131:861-872
- ↑ Junying Yu, Maxim A. Vodyanik, Kim Sumuga-Otto, Jessica Antosiewicz-Bourget, Jeniffer L. Frane, Shulan Tian, Jeff Nie, Gurdrun A. Jonsdottir, Victor Ruotti, Ron Stewart, Igor I. Slukvin, and James A. Thomson (2007). Induced Pluripotent stem cell lines derived from human somatic cells.. Science 21 December 2007: 1917-1920
- ↑ http://bloodjournal.hematologylibrary.org/content/114/27.abstract.pdf
- ↑ http://app.yonhapnews.co.kr/YNA/Basic/article/new_search/YIBW_showSearchArticle_New.aspx?searchpart=article&searchtext=%EC%84%B1%EC%B2%B4%EC%A4%84%EA%B8%B0%EC%84%B8%ED%8F%AC+%EB%B6%84%ED%99%94%EC%A1%B0%EC%A0%88+%EC%9C%A0%EC%A0%84%EC%9E%90%EF%BF%BD%EC%9B%90%EB%A6%AC+%EB%B0%9D%ED%98%80&contents_id=AKR20111110102500017[깨진 링크(과거 내용 찾기)]
- ↑ Fernandez, P.C., Frank, S.R., Wang, L., Schroeder, M., Liu, S., Greene,J., Cocito, A. and Amati, B. (2003). Genomic targets of the human c-Myc protein. Genes Dev. 17, 1115-1129
- ↑ Rowland, B.D., Bernards, R., and Peeper, D.S. (2005). The KLF4 tumour suppressor is a transcriptional repressor of p53 that acts as a context-dependent oncogene. Nat. Cell Biol. 7, 1074-1082
- ↑ Lin, T., Chao, C., Saito, S., Mazur, S.J., Murphy, M.E., Appella, E., and Xu, Y. (2004) p53 induces differentiation of mouse embryonic stem cells by suppressing Nanog expression. Nat. Cell Biol. 7, 165-171. Published Online December 26, 2004. 10.1038/ncb1211
- ↑ Takahashi K, Yamanaka S(2006). Induction of pluripotent stem cells from mouse embryonic and adult fibroblast cultures by defined factors. Cell 126: 663-676
- ↑ http://www.sciencemag.org/content/322/5903/949.abstract
- ↑ Nakagawa, Masato Koyanagi, Michiyo Tanabe, Kazutoshi Takahashi, Kazutoshi Ichisaka, Tomoko Aoi, Takashi Okita, Keisuke Mochiduki, Yuji Takizawa, Nanako Yamanaka, Shinya(2008). Generation of induced pluripotent stem cells without Myc from mouse and human fibroblasts. Nature biotechnology / v.26 no.1, 2008년, pp.101-106
- ↑ http://www.hellodd.com/kr/dd_news/article_view.asp?mark=36443[깨진 링크(과거 내용 찾기)]
- ↑ Lee G, Papapetrou EP, Kim H, Chambers SM, Tomishima MJ, Fansano CA, et al (2009). Modeling pathogenesis and treatment of familial dysautonomia using patient-specific iPSCs. Nature 461:402-406
- ↑ Itzhaki I, Maizel L, Huber I, Zwi-Dantsis L, Caspi O, Winterstern A et al (2011). Modelling the long QT syndrome with induced pluripotent stem cells. Nature 461
- ↑ 배아줄기세포로 정자 만들었다, 경향신문, 2009-07-08
- ↑ 쥐의 줄기세포로 만든 정자 수정 새끼쥐 낳았다, 한국일보, 2011-08-05
- ↑ 美, 무정자증 남성 피부세포로 정자 만들어…`깜짝`, 매일경제, 2014-05-05
- ↑ “김영진. "유도만능줄기세포의 현재와 전망." 국내석사학위논문 고려대학교 의학전문대학원, 2014. 서울”.
참고 문헌[편집]
- 황동연(2008), 「역분화 만능 줄기세포」, 『분자세포생물학뉴스』, Vol. 20, 24~35면.
- http://www.sciencemag.org/cgi/content/abstract/1164270v1
- http://www.jpnews.kr/sub_read.html?uid=10642
- http://www.sciencedirect.com/science/article/pii/S0959437X12000676
- http://www.nobelprize.org/nobel_prizes/medicine/laureates/2012/#
- https://web.archive.org/web/20160304103446/http://www.ksmbmb.or.kr/ksbmb_webzine/webzine.php?sub=4&vol=12&Location=View
같이 보기[편집]
- 동의어
