원자가 껍질 전자쌍 반발 이론
이 문서의 내용은 출처가 분명하지 않습니다. (2014년 9월) |

원자가껍질 전자쌍 반발 이론(Valence shell electron pair repulsion theory : VSEPR theory)이란 화학에서 중심원자의 배위수와 전자쌍 반발 원리를 통해 분자의 구조를 예측, 나타내는 모형이다.[1](루이스 구조식에서 비공유 전자쌍을 나타내주어야 한다)
이 이론은 루이스 구조에서 나타나는 중심원자의 각 전자쌍들은 서로 반발하므로 서로 가장 멀리 떨어진 위치에 존재하게 된다는 것에 기초하여 분자의 구조를 나타낸다. 예를 들어 중심원자에 3개의 전자쌍이 존재한다면 각 전자쌍은 중심원자를 중심으로 정삼각형의 형태로 위치하게 되는 것이다. 분자를 구성하는 원자들은 결합전자쌍을 통해 결합하고 있으므로 결합전자쌍의 배치가 곧 분자의 모양이 된다.
전자쌍에는 결합전자쌍과 비공유전자쌍(비결합전자쌍)이 있는데 결합전자쌍보다 비공유전자쌍의 반발력이 더 크다. 따라서 비공유-비공유 전자쌍 간의 반발력이 가장 크며 결합-결합 전자쌍 간의 반발력이 가장 작다. 따라서 같은 개수의 전자쌍을 갖고 있더라도 결합전자쌍과 비공유전자쌍의 구성에 따라 각 전자쌍들이 이루는 각은 조금씩 달라질 수 있다.
역사[편집]
1940년 분자기하학과 원자가전자 사이의 관계에 대한 첫번째 모델이 제기되었으며,[2] 1957년 로널드 길레스피와 로널드 시드니 니홈에 의해 더 발전하였다.[3][4]
입체수와 비결합전자쌍 수에 따른 분자의 모양[편집]
입체수(Steric Number, 결합수 + 비결합전자쌍의 수)와 비결합전자쌍의 수에 따른 분자의 모양은 다음과 같다.
| 입체수 | 분자기하 [5] 비공유전자쌍 없음 |
분자기하 [6]:413–414비공유전자쌍 |
분자기하 비공유전자쌍 4개 | |
|---|---|---|---|---|
| 2 | ||||
| 3 |  |
 |
||
| 4 | 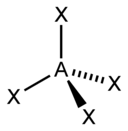 |
 |
 |
|
| 5 |  |
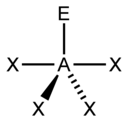 |
 |
 3) |
| 6 | 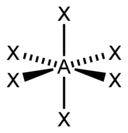 |
 |
 |
|
| 7 |  |
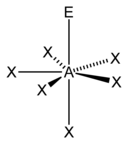 5)[8] |
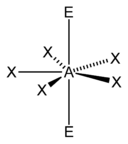 5)[9]:498 |
|
| 8 |  (TaF3− |
|||
| 9 | 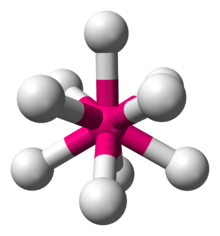 세모자쓴 삼각기둥형 (ReH2− 세모자쓴 삼각기둥형 (ReH2−9)[9]:254 |
같이 보기[편집]
각주[편집]
- ↑ Jolly, W. L. (1984). 《Modern Inorganic Chemistry》. McGraw-Hill. 77–90쪽. ISBN 0-07-032760-2.
- ↑ Sidgwick, N. V.; Powell, H. M. (1940). “Bakerian Lecture. Stereochemical Types and Valency Groups”. 《Proc. Roy. Soc. A》 176: 153–180. doi:10.1098/rspa.1940.0084.
- ↑ Gillespie, R. J.; Nyholm, R. S. (1957). “Inorganic stereochemistry”. 《Quart. Rev. Chem. Soc.》 11: 339. doi:10.1039/QR9571100339.
- ↑ Gillespie, R. J. (1970). “The electron-pair repulsion model for molecular geometry”. 《J. Chem. Educ.》 47 (1): 18. doi:10.1021/ed047p18.
- ↑ Petrucci, R. H.; W. S., Harwood; F. G., Herring (2002). 《General Chemistry: Principles and Modern Applications》 8판. Prentice-Hall. 413–414 (Table 11.1)쪽. ISBN 978-0-13-014329-7.
- ↑ Petrucci, R. H.; W. S., Harwood; F. G., Herring (2002). 《General Chemistry: Principles and Modern Applications》 8판. Prentice-Hall. ISBN 978-0-13-014329-7.
- ↑ 가 나 Miessler, G. L.; Tarr, D. A. (1999). 《Inorganic Chemistry》 2판. Prentice-Hall. 54–62쪽. ISBN 978-0-13-841891-5.
- ↑ Baran, E. (2000). “Mean amplitudes of vibration of the pentagonal pyramidal XeOF−
5 and IOF2−
5 anions”. 《J. Fluorine Chem.》 101: 61–63. doi:10.1016/S0022-1139(99)00194-3. - ↑ 가 나 Housecroft, C. E.; Sharpe, A. G. (2005). 《Inorganic Chemistry》 2판. Pearson. ISBN 978-0-130-39913-7.
