우르소데옥시콜산
| |

| |
| 체계적 명칭 (IUPAC 명명법) | |
|---|---|
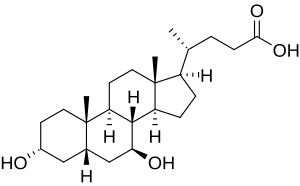
| 3α,7β-dihydroxy-5β-cholan-24-oic acid OR (R)-4-((3R,5S,7S,8R,9S,10S,13R,14S,17R)-3,7-dihydroxy- 10,13-dimethylhexadecahydro- 1H-cyclopenta[a]phenanthren-17-yl)pentanoic acid | |
| 식별 정보 | |
| CAS 등록번호 | 128-13-2 |
| ATC 코드 | A05AA02 |
| PubChem | 31401 |
| 드러그뱅크 | DB01586 |
| ChemSpider | 29131 |
| 화학적 성질 | |
| 화학식 | C24H40O4 |
| 분자량 | 392.56 |
| 유의어 | Ursodiol |
| 물리적 성질 | |
| 녹는점 | 203 °C (397 °F) |
| 약동학 정보 | |
| 생체적합성 | ? |
| 동등생물의약품 | ? |
| 약물 대사 | ? |
| 생물학적 반감기 | ? |
| 배출 | ? |
| 처방 주의사항 | |
| 허가 정보 | |
| 임부투여안전성 | B3(오스트레일리아) ?(미국) |
| 법적 상태 | |
| 투여 방법 | By mouth |

우르소데옥시콜산(Ursodeoxycholic acid, UDCA)은 간에서 합성되어 담즙으로 배설된 뒤 장내 미생물에 의해 대사를 받은 후 간으로 재흡수(장간재순환, enterohepatic recirculation)되는 3차 담즙산이다.[2]
작용기전[3][편집]
| UDCA[4] | |
|---|---|
| 구조식 | C24H40O4 |
| 분자량 | 392.58 g/mol |
| 녹는점 | 203°C |
담즙울체성 질환(cholestatic disease)에 대한 UDCA의 작용기전은 아직 명확히 밝혀지지 않았다. 담즙울체성 간질환은 소수성 담즙산(chenodeoxycholic acid, deoxycholic acid, lithocholic acid)이 간에 축적되어 발생하는데, 이 축적된 담즙산은 계면활성(detergent) 작용을 통해 간세포를 손상시키고, 이로써 간세포의 자멸사(apoptosis)가 나타난다. UDCA는 친수성·무독성 담즙산으로 세포막과 세포 소기관으로부터 소수성 독성 담즙산 분자를 경쟁적으로 제거함으로써, 이들 독성 담즙산이 간세포와 담관세포에 일으키는 손상을 예방하는 작용을 한다.[3] 또한, UDCA는 소수성 담즙산의 소장 흡수를 경쟁적으로 저해함으로써 혈청과 담즙 내의 UDCA 비율을 증가시킨다. 그 밖에 원발 쓸개관 간경화(PBC, primary biliary cirrhosis) 및 원발 경화성 담관염(PSC, primary sclerosing cholangitis) 환자에서, 담즙산, 인지질 및 콜레스테롤의 분비를 돕는 역할을 한다.[3]
세포 보호 효과[편집]
UDCA는 간에서 글리신이나 타우린과 포합체(conjugates)를 형성한다. 이 포합체는 소수성 담즙산에 의한 간세포의 용해(cytolysis)를 현저히 감소시킨다. 최근, 쥐를 이용한 연구에서 UDCA가 독성 담즙산으로 인한 세포자멸사(apoptosis)를 억제함이 밝혀졌다. 또한, UDCA는 세포자멸사에 관여하는 p53 경로를 억제하여 세포보호 작용을 나타낸다고 보고되었다.[3]
세포막안정화 효과[편집]
독성 담즙산은 세포막의 무극성 영역(apolar domain)의 극성을 증가시키는데, 친수성인UDCA와 UDCA포합체는 세포막의 극성을 감소시킴으로써, 소수성 담즙산의 계면활성작용에 의한 세포막 손상을 예방한다. 즉 UDCA는 소수성 담즙산에 의한 세포막 손상을 예방한다.[3]
항산화 효과[편집]
독성 담즙산은 간의 쿠퍼세포(Kuffer’s cells)를 활성화하여 활성산소들(reactive oxygen species)의 생성을 촉진한다. 활성산소는 지질과산화 과정을 통해 간세포를 손상시키는데, UDCA는 독성 담즙산에 의한 쿠퍼세포의 활성화를 억제함으로써, 항산화 효과를 나타낸다. 또한 UDCA는 간세포 내의 글루타치온(glutathione) 농도와 티올(thiol)기를 함유한 단백질의 농도를 증가시킴으로써 간세포의 산화적 손상에 대한 보호작용을 하기도 한다. 최근에는 Nrf2 전사인자 매개에 의해 UDCA의 항산화 효과가 나타난다고 보고되었다.[3]
면역조절 효과[편집]
HLA(=Human Leucocyte Antigen)는 인간의 중요한 조직적합성 항원으로 주조직적합복합체(MHC, Major Histocompatibility Complex)를 형성하는데, 모든 조직의 세포막에 존재하고 있으며, 자기와 비자기를 구분하는 역할을 한다. 바이러스나 세균이 세포 내에서 증식하면 MHC Class Ⅰ, Ⅱ항원은 이 감염된 세포와 결합함으로써 T세포에게 세포감염을 알리는 역할을 한다. 원발성담즙경화증 (PBC, Primary Biliary Cirrhosis) 환자나 간장 밖의 담즙정체(extra-hepatic cholestasis) 환자는 간세포와 담관에서 HLA class Ⅰ과 Ⅱ 항원의 발현이 증가된다. CDCA 및 다른 소수성 담즙산은 MHC class Ⅰ과 Ⅱ항원의 발현을 증가시키는데, UDCA는 담즙산에서 소수성 담즙산을 대체하기 때문에 소수성 담즙산에 의한 MHC 유전자의 발현을 감소시켜 면역을 조절하는 역할을 한다.[3]
임상 적응증(medical uses)[5][편집]
UDCA는 PBC치료제로는 유일하게 FDA의 승인을 받은 성분이다. 또한 담석을 용해시키는 효능이 있어 FDA에서 1987년 담석증 치료제로 승인 받았고, 1996년에 급격히 체중을 감소한 비만 환자의 담석예방제로 승인받은 성분이다. 그 밖에PSC(=Primary Sclerosing Cholangitis, 원발경화성담관염), 임신부의 간내 담즙정체(intrahepatic cholestasis), 낭포성 섬유증(cystic fibrosis)과 관련된 간질환, 비알코올성 지방간, 대숙주성 이식편병(graft-versus-host disease), 수액을 통한 종합 비경구 영양(total parenteral nutrition)으로 인한 담즙울혈(cholestasis) 및 일부 담즙울체성 소아 간질환 등에서 비정상적인 간기능 수치를 유의하게 개선시킨다.
제품[편집]
UDCA 단일제로는 대웅제약의 우루사정200mg, 300mg 등이 있고, 복합제로는 대웅제약의 대웅우루사연질캡슐, 복합우루사연질캡슐 등이 있다.
각주[편집]
- ↑ “Ursodeoxycholic acid 300mg Tablets - Summary of Product Characteristics (SmPC)”. 《(emc)》. 2019년 7월 10일. 2020년 4월 29일에 확인함.
- ↑ Martin FP, et al. Mol Syst Biol. 2007;3:112.
- ↑ 가 나 다 라 마 바 사 Kumar D, et al. J Gastroenterol Hepatol. 2001;16(1):3-14.
- ↑ The Merck Index. 15th ed. RSC publishing. 2013.
- ↑ Angulo P. Curr Gastroenterol Rep. 2002;4(1):37-44.
