뇌전도
| 뇌전도 | |
|---|---|
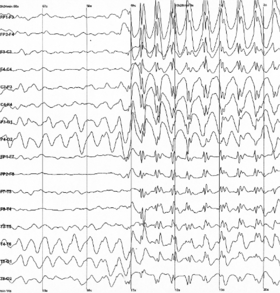 뇌전증 발작시 나타나는 스파이크 |
뇌전도(腦電圖, 영어: electroencephalogram(데이터), electroencephalography(기술), EEG)는 전극을 통해 뇌의 전기적 활동을 기록하는 전기생리학적 측정방법을 말한다. 일반적으로 두피에 전극을 부착하여 신호를 측정하는 경우만 가리켜 말한다. 신경 세포 내부에서 발생하는 이온 전류에 의해 유도된 전위의 요동을 측정하는 것이다.[1] 환자를 진단할 때에는 주로 특정 사건이 일어날 때 발생하는 사건 관련 전위나, 뇌파의 스펙트럼 밀도를 주로 분석한다.
뇌전증 환자를 대부분 뇌전도의 이상을 통해 진단한다.[2] 이외에도 수면 장애, 혼수상태, 뇌증, 뇌사를 진단할 때 사용하기도 하며 마취의 깊이를 측정할 때에도 사용될 수 있다. 뇌종양이나 뇌졸중이 의심될 때 가장 처음으로 진단할 수 있는 도구이기도 하지만, 자기공명영상이나 컴퓨터단층촬영 등 해부학적 정보를 쉽게 볼 수 있는 방식이 개발되고 난 이후로는 잘 사용되지 않는다.[3][4] 공간분해능이 별로 좋지는 않지만, 밀리초 단위의 시간분해능을 가지고 있다는 특징 때문에 여전히 연구되고 사용되는 도구이기도 하다.
뇌 손상, 뇌전증 또는 여러 질환을 평가하는 거나, 법률적으로 뇌사를 진단하는 데 사용한다. 다른 종류의 뇌영상화 시스템과 함께 사용할 수 있다.
역사[편집]


1875년, 리버풀 출신의 의사 리처드 카튼은 토끼와 원숭이의 대뇌에서 전기적 현상이 발생한다는 사실을 발견해 《영국의학저널》에 발표한다. 1890년에는 폴란드의 생리학자인 아돌프 벡이 토끼와 개의 대뇌에서 발생하는 전기신호의 주기가 빛의 색에 따라 달리잔다는 것을 발견한다. 이 발견에 깊은 인상을 받은 벡은 전극을 동물의 뇌에 부착하여 여러 가지 자극에 따라 어떻게 신호가 달라지는지를 연구한다. 이러한 탐구는 이후 뇌파가 발견되는데 지대한 공헌을 끼쳤다.[5]
1912년에는 우크라이나의 생리학자인 블라디미르 프라디치-네민스키가 개에게서 뇌파를 측정하여 유발전위를 발견한다.[6] 1914년에는 나폴레온 시불스키가 발작을 유도하여 발작중의 뇌전도를 측정한다.
독일의 생리학자이자 정신과의인 한스 베르거는 1924년에 처음으로 사람의 뇌파를 기록한다.[7] 베르거는 뇌전도를 측정하는 기구를 발명하고, 최초로 뇌전도라는 이름을 붙인다.[8] 이 발견은 이후 에드거 에이드리언 등에 의해 검증되고 연구된다.
1934년에는 간질환자가 발작중에 뇌전도상에서 스파이크가 발생한다는 사실이 보고되었고, 1935년에는 결신 발작중에도 뇌파에서 특이한 규칙성이 관찰된다는 것이 알려졌다.[9] 이 두 연구를 기점으로 뇌전도가 임상 영역에서 널리 사용되기 시작한다. 이듬해 매사추세츠 종합병원에서 뇌전도 연구실이 개원한다.
1950년대 영국 내과의사 윌리엄 그레이 월터는 어디서 어떤 뇌파가 측정되었는지를 나타내는 뇌전도 지도(EEG topography)라는 기술을 개발한다. 이 기술은 1980년대에 임상적으로 잠깐 사용된 이후로 현재는 학계에서 주로 사용된다.
뇌파와의 관계[편집]
뇌파는 뇌의 신경신호들이 만들어내는 파동 형태로 분석 가능한 신호를 의미하는 반면, 뇌전도는 이 뇌파를 두피 위에 전극을 부착하여 비침습적으로 측정해 낸 일련의 신호 또는 측정 행위를 의미한다. 그러나 뇌전도와 뇌파라는 용어는 현재까지도 많이 혼용되고 있다. 뇌파(腦波)라는 단어는 1942년 나고야 대학 의학부의 카츠누마 세이조에 의해 처음으로 제안된다. 당시에는 뇌파를 측정한다는 것은 뇌전도를 측정한다는 것과 동일하여 구분할 필요가 없었으나, 이후 1950년에 피질전도의 개념이 제안되며 이 둘을 구분할 필요가 생겼지만 기존의 언어관습이 그대로 굳어져 뇌전도를 구분하지 않고 현재까지도 뇌파라는 단어를 무분별하게 사용하는 경우가 많다.[10]
기작[편집]
뇌 속에 있는 수십억개의 신경 세포들은 흥분을 반복하며 전하의 흐름을 만들어낸다.[11] 신경 세포들은 이온을 수송하는 막수송단백질들로 인해 평상시에 휴지 전위를 띄는데, 이를 분극되었다고 한다. 정상 상태의 신경 세포는 신호가 들어오면 탈분극과 과분극을 통해 신호를 전달하는데, 이를 활동전위라고 한다. 이처럼 신호가 전달될 때 신경 세포로부터 빠져나온 이온들은 그 주변에 있는 또 다른 이온들을 정전기적 척력으로 밀어내게 되고, 이러한 과정이 연쇄적으로 일어나면서 일종의 파동이 발생한다. 이처럼 이온의 입체적 이동을 용적 전도(volume conduction)라 한다. 이러한 이온의 움직임이 전자를 밀고 당김으로써 전하의 움직임은 두피에 부착된 금속 전극에도 전파될 수 있다. 금속에 있는 자유전자들이 이런 전기장의 변화에 따라 움직임으로써 전극은 전압계의 기능을 하게 된다.[12]
신경 세포 하나가 만드는 전기적 위치 에너지는 너무나도 작아서 뇌전도나 뇌자도로 측정하는 것이 불가능하다.[13] 그러므로 뇌전도는 신경 세포 하나하나의 신호를 포착하는 것이 아닌, 동기화된 수천~수백만 신경 세포들의 활동을 종합하여 측정하는 것이다. 이러한 동기화는 신경 세포들이 같은 방향으로 배치되어 각 세포의 이온 이동이 다른 세포에 영향을 주기 때문에 나타난다. 이런 점을 감안했을 때, 정렬되어 동시에 활성되는 경우가 많은 대뇌 피질에 있는 원추세포들이 대부분의 뇌전도 신호를 일으키는 것으로 여겨진다. 전기적 위치 에너지가 거리의 제곱에 반비례하기 때문에 뇌 심부에서 발생한 신호는 거의 측정되지 않는다.[14]
측정된 뇌전도는 뇌파에 다양한 주파수 성분이 존재함을 보여준다. 특히 특정 주파수 대역이 크게 관찰되며, 뇌의 상태에 따라 이러한 주파수 대역의 세기가 서로 달라지는 것이 알려져 있다. 특정 주파수 대역이 강하게 관측되는 원인으로 해부학적 요인이 지목되지만, 시상에 존재하는 수면 방추의 공명현상을 제외하고는 거의 알려진 바가 없다. 감마파와 델타파의 상관관계가 잘 알려져 있다.[15]
연구 방법론[편집]
뇌전도는 사건 관련 전위에 대한 연구에서 애용되므로 신경과학, 인지과학, 인지심리학, 신경언어학, 심리생리학 등 넓은 분야에서 연구 방법론 중 하나로 꾸준히 사용된다.[16][17][18] 그러나 사건 관련 전위에 대한 연구들의 재현성이 낮기 때문에 아직까지 의료계에서 더 다양한 방식으로 임상응용하기에는 충분치 못하다는 평가를 받고 있다.[19] 하지만 중추청각처리장애(APD)나 주의력결핍 과다행동장애(ADHD) 등 일부 정신과적 장애를 다루는데에는 보다 널리 사용되는 추세이다.
장점[편집]
fMRI, PET, 뇌자도 등 다른 뇌영상 기술과 비교할 때 뇌전도가 가지는 장점은 다음과 같다.
- MRI같은 경우 수억원을 호가하는데 비해 뇌전도는 기구의 가격이 저렴하다.[20]
- 운용에 특별한 기술자가 필요하지 않아 응급상황에 편리하다.[21]
- 뇌자도는 수십억원어치의 장비와 액체 헬륨을 필요로 하고, MRI는 1톤짜리 전자석을 필요로 하는데 비해 뇌전도는 특별한 기구가 필요하지 않아서 사용할 수 있는 환경에 제약이 거의 없다.[22]
- 시간분해능이 매우 좋다. 시판되는 기구로는 250~2000 Hz의 신호를 측정할 수 있으며, 연구실에서 개발중인 도구는 20,000 Hz 역시 측정할 수 있다. 뇌자도와 사건관련광신호(Event-related Optical Signall; EROS) 역시 이와 비슷한 정도의 시간분해능을 가진다.[22]
- 피험자의 움직임에 영향을 비교적 덜 받으며, 그나마도 상쇄시키는 기술이 많이 개발되었다.[23]
- 소리가 나지 않아 청각과 관련된 오차신호가 덜 발생한다.
- 폐소공포증 환자도 사용 가능하다.[24]
- 강한 자기장을 필요로 하지 않아 심박조율기 등 금속 보철물을 삽입한 환자에게도 적용 가능하다.[25]
- 방사선을 사용하지 않는다.[26]
- 원리가 간단하다.
- 두피 겉면에 부착하여 침습적 피해가 전혀 없다.
행동 연구를 할 때에는 다음의 특징들이 특히 매력적이다.
- 외부로 반응이 나타나지 않는 신호에 대해서도 연구할 수 있다.[27]
- 운동반응을 할 수 없는 피험자에게도 적용 가능하다.[28]
- 피험자가 자극에 집중하지 않아도 감지할 수 있는 경우도 있다.
- 나이를 먹어감에 따라서 뇌의 신호가 바뀐다.[29]
단점[편집]
- fMRI 등에 비해 공간분해능이 낮다.[30]
- 대뇌 피질 밑에서 발생하는 신호는 감지하기 어렵다.
- PET나 MRS와는 다르게 신경전달물질의 종류를 알 수 없다.[26]
- 두피의 정확한 위치에 전극을 위치시켜야하며, 전도성이 있는 젤이 계속 증발한다.
- 노이즈가 너무 많아 통계적으로 유의미한 정보를 얻기 위해서는 다량의 데이터가 필요하다.[31]
다른 신경영상법과 함께[편집]
뇌전도와 fMRI를 동시에 측정함으로써 좋은 성과를 얻고 있다.[32][33][34][35] 그러나 이 둘을 동시에 사용하기 위해서는 심탄동계적 아티팩트, MRI 펄스 아티팩트, 그리고 뇌전도를 측정하는 전선이 강한 자기장 내에서 움직이는 현상에서 오는 아티팩트 등 다양한 문제를 해결해야 할 필요가 있다. 그러나 이런 문제들은 여러 가지 연구를 통해 그 해결방식이 제안된 상태다.[36][37]
뇌자도도 같이 측정되는 경우가 많다. 이 둘을 동시에 사용함으로써 연구자들이 얻을 수 있는 효과는 다음과 같다.
- 뇌전도는 두개골의 반지름, 두개골의 전기전도도 등 다양한 요소를 고려해야 하는 반면 뇌자도의 경우는 그렇지 않기 때문에 복잡하고 부정확한 역연산을 필요로 하지 않는다.
- 뇌자도 역시 뇌전도와 마찬가지로 뇌의 심부로 갈수록 그 정확한 복원이 힘들어지지만, 그래도 두 기술을 병용함으로써 둘 중 하나만 사용하는 것 보다는 더 많은 노이즈를 제거할 수 있어서 정확한 뇌 심부 이미지를 얻는데 용이하다.
- 뇌자도는 과학적인 한계때문에 대뇌 피질에서 몇 cm만 내려가더라도 정확한 영상을 얻을 수 없다. 하지만 뇌전도는 비록 노이즈가 있지만 피질 하부의 정보를 얻는 것이 가능하다. 따라서 뇌자도를 통해 어떤 신호가 대뇌 피질에서 형성되었는지를 알 수 있고, 뇌전도를 통해 좀더 깊은 곳에서 생긴 신호를 측정하는 것이 가능하다.[38]
이러한 까닭에 뇌전증 연구 등에서 뇌전도(EEG)와 뇌자도(MEG)를 종합한 뇌전자도(EMEG)가 최근들어 많이 사용되기 시작했다.[39]
뇌전도는 양전자 방출 단층촬영(PET)과도 함께 사용될 수 있다. 이를 통해 PET로 약물이 작용하는 부위를 관찰함으로써 그 부위에서 발생하는 뇌전도 신호를 분석할 수 있다.[40]
최근에는 전두엽에서 측정한 뇌전도 데이터를 기계 학습을 통해 사람의 심리 상태를 통계적으로 분류하는 연구가 이루어졌는데, 높은 정확도를 보여 학계의 주목을 받고 있다.[41][42][43]
방법[편집]
일반적으로 임피던스를 줄이기 위해 머리를 가볍게 깎고, 전도성 젤을 바른 부위에 전극을 부착한다. 각각의 전극은 앰프에 연결한다. 앰프는 전압을 1천배에서 10만배까지 증폭한다. 이렇게 증폭된 전류는 스크린에 표시되거나 컴퓨터에 입력된다. 뇌전도의 전위는 두피에서 측정했을 때 약 100µV, 피질에서 측정했을 때 약 1-2 mV이다. 피질에서 측정하는 경우를 피질전도(ECoG)로, 전극을 깊숙이 꽂아 측정하는 경우를 입체전도(sEEG)라 부른다.
전극과 앰프를 연결하는 방법에는 다음의 세 가지가 있다.
- Common reference derivation
- Average reference derivation
- Bipolar derivation
각주[편집]
- ↑ Niedermeyer E.; da Silva F.L. (2004). 《Electroencephalography: Basic Principles, Clinical Applications, and Related Fields》. Lippincott Williams & Wilkins. ISBN 978-0-7817-5126-1.
- ↑ Tatum, William O. (2014). 《Handbook of EEG interpretation》. Demos Medical Publishing. 155–190쪽. ISBN 9781617051807. OCLC 874563370.
- ↑ “EEG”.
- ↑ Chernecky, Cynthia C.; Berger, Barbara J. (2013). 《Laboratory tests and diagnostic procedures》 6판. St. Louis, Mo.: Elsevier. ISBN 9781455706945.
- ↑ Coenen, Anton; Edward Fine; Oksana Zayachkivska (2014). “Adolf Beck: A Forgotten Pioneer In Electroencephalography”. 《Journal of the History of the Neurosciences》 23 (3): 276–286. doi:10.1080/0964704x.2013.867600. PMID 24735457. S2CID 205664545.
- ↑ Pravdich-Neminsky, VV. (1913). “Ein Versuch der Registrierung der elektrischen Gehirnerscheinungen”. 《Zentralblatt für Physiologie》 27: 951–60.
- ↑ Haas, L F (2003). “Hans Berger (1873-1941), Richard Caton (1842-1926), and electroencephalography”. 《Journal of Neurology, Neurosurgery & Psychiatry》 74 (1): 9. doi:10.1136/jnnp.74.1.9. PMC 1738204. PMID 12486257.
- ↑ Millet, David (2002). "The Origins of EEG". Archived 2020년 9월 8일 - 웨이백 머신 International Society for the History of the Neurosciences (ISHN).
- ↑ GIBBS, F. A. (1935년 12월 1일). “THE ELECTRO-ENCEPHALOGRAM IN EPILEPSY AND IN CONDITIONS OF IMPAIRED CONSCIOUSNESS”. 《Archives of Neurology And Psychiatry》 34 (6): 1133. doi:10.1001/archneurpsyc.1935.02250240002001. ISSN 0096-6754.
- ↑ Palmini, A (2006). “The concept of the epileptogenic zone: A modern look at Penfield and Jasper's views on the role of interictal spikes”. 《Epileptic Disorders》 8 (Suppl 2): S10–5. PMID 17012068.
- ↑ Herculano-Houzel S (2009). “The Human Brain in Numbers”. 《Frontiers in Human Neuroscience》 3: 31. doi:10.3389/neuro.09.031.2009. PMC 2776484. PMID 19915731.
- ↑ Tatum, W. O., Husain, A. M., Benbadis, S. R. (2008) "Handbook of EEG Interpretation" Demos Medical Publishing.
- ↑ Nunez PL, Srinivasan R (1981). 《Electric fields of the brain: The neurophysics of EEG》. Oxford University Press. ISBN 9780195027969.
- ↑ Klein, S.; Thorne, B. M. (2006년 10월 3일). 《Biological psychology》. New York, N.Y.: Worth. ISBN 978-0-7167-9922-1.
- ↑ Whittingstall, Kevin; Logothetis, Nikos K. (2009). “Frequency-Band Coupling in Surface EEG Reflects Spiking Activity in Monkey Visual Cortex”. 《Neuron》 64 (2): 281–9. doi:10.1016/j.neuron.2009.08.016. PMID 19874794. S2CID 17650488.
- ↑ Yang, H.; Ang, K.K.; Wang, C.; Phua, K.S.; Guan, C. (2016), “Neural and cortical analysis of swallowing and detection of motor imagery of swallow for dysphagia rehabilitation—A review”, 《Progress in Brain Research》 228: 185–219, doi:10.1016/bs.pbr.2016.03.014, ISBN 9780128042168, PMID 27590970
- ↑ Jestrović, Iva; Coyle, James L; Sejdić, Ervin (2015년 9월 15일). “Decoding human swallowing via electroencephalography: a state-of-the-art review”. 《Journal of Neural Engineering》 12 (5): 051001. Bibcode:2015JNEng..12e1001J. doi:10.1088/1741-2560/12/5/051001. ISSN 1741-2560. PMC 4596245. PMID 26372528.
- ↑ Cuellar, M.; Harkrider, A.W.; Jenson, D.; Thornton, D.; Bowers, A.; Saltuklaroglu, T. (July 2016). “Time–frequency analysis of the EEG mu rhythm as a measure of sensorimotor integration in the later stages of swallowing”. 《Clinical Neurophysiology》 127 (7): 2625–2635. doi:10.1016/j.clinph.2016.04.027. ISSN 1388-2457. PMID 27291882. S2CID 3746307.
- ↑ Clayson, Peter E.; Carbine, Kaylie A.; Baldwin, Scott A.; Larson, Michael J. (2019). “Methodological reporting behavior, sample sizes, and statistical power in studies of event-related potentials: Barriers to reproducibility and replicability”. 《Psychophysiology》 (영어) 56 (11): e13437. doi:10.1111/psyp.13437. ISSN 1469-8986. PMID 31322285.
- ↑ Vespa, Paul M.; Nenov, Val; Nuwer, Marc R. (1999). “Continuous EEG Monitoring in the Intensive Care Unit: Early Findings and Clinical Efficacy”. 《Journal of Clinical Neurophysiology》 16 (1): 1–13. doi:10.1097/00004691-199901000-00001. PMID 10082088.
- ↑ Schultz, Teal L. (2012). “Technical Tips: MRI Compatible EEG Electrodes: Advantages, Disadvantages, And Financial Feasibility In A Clinical Setting”. 《Neurodiagnostic Journal 52.1》 52 (1): 69–81. PMID 22558648.
- ↑ 가 나 Hämäläinen, Matti; Hari, Riitta; Ilmoniemi, Risto J.; Knuutila, Jukka; Lounasmaa, Olli V. (1993). “Magnetoencephalography-theory, instrumentation, and applications to noninvasive studies of the working human brain”. 《Reviews of Modern Physics》 65 (2): 413–97. Bibcode:1993RvMP...65..413H. doi:10.1103/RevModPhys.65.413.
- ↑ O'Regan, S; Faul, S; Marnane, W (2010). 〈Automatic detection of EEG artifacts arising from head movements〉. 《2010 Annual International Conference of the IEEE Engineering in Medicine and Biology》. 6353–6쪽. doi:10.1109/IEMBS.2010.5627282. ISBN 978-1-4244-4123-5.
- ↑ Murphy, Kieran J.; Brunberg, James A. (1997). “Adult claustrophobia, anxiety and sedation in MRI”. 《Magnetic Resonance Imaging》 15 (1): 51–4. doi:10.1016/S0730-725X(96)00351-7. PMID 9084025.
- ↑ Schenck, John F. (1996). “The role of magnetic susceptibility in magnetic resonance imaging: MRI magnetic compatibility of the first and second kinds”. 《Medical Physics》 23 (6): 815–50. Bibcode:1996MedPh..23..815S. doi:10.1118/1.597854. PMID 8798169.
- ↑ 가 나 Yasuno, Fumihiko; Brown, Amira K; Zoghbi, Sami S; Krushinski, Joseph H; Chernet, Eyassu; Tauscher, Johannes; Schaus, John M; Phebus, Lee A; Chesterfield, Amy K; Felder, Christian C; Gladding, Robert L; Hong, Jinsoo; Halldin, Christer; Pike, Victor W; Innis, Robert B (2007). “The PET Radioligand \11C]MePPEP Binds Reversibly and with High Specific Signal to Cannabinoid CB1 Receptors in Nonhuman Primate Brain”. 《Neuropsychopharmacology》 33 (2): 259–69. doi:10.1038/sj.npp.1301402. PMID 17392732.
- ↑ Mulholland, Thomas (2012). 〈Objective EEG Methods for Studying Covert Shifts of Visual Attention〉. McGuigan, F. J.; Schoonover, R. A. 《The Psychophysiology of Thinking: Studies of Covert Processes》. 109–51쪽. ISBN 978-0-323-14700-2.
- ↑ Hinterberger, Thilo; Kübler, Andrea; Kaiser, Jochen; Neumann, Nicola; Birbaumer, Niels (2003). “A brain–computer interface (BCI) for the locked-in: Comparison of different EEG classifications for the thought translation device”. 《Clinical Neurophysiology》 114 (3): 416–25. doi:10.1016/S1388-2457(02)00411-X. PMID 12705422. S2CID 11857440.
- ↑ Feinberg, I.; Campbell, I. G. (2012). “Longitudinal sleep EEG trajectories indicate complex patterns of adolescent brain maturation”. 《AJP: Regulatory, Integrative and Comparative Physiology》 304 (4): R296–303. doi:10.1152/ajpregu.00422.2012. PMC 3567357. PMID 23193115. 요약문 – ScienceDaily (2013년 3월 19일).
- ↑ Srinivasan, Ramesh (1999). “Methods to Improve the Spatial Resolution of EEG”. 《International Journal》 1 (1): 102–11.
- ↑ Schlögl, Alois; Slater, Mel; Pfurtscheller, Gert (2002). “Presence research and EEG” (PDF).
- ↑ Huang-Hellinger, F.; Breiter, H.; McCormack, G.; Cohen, M.; Kwong, K. (1995). “Simultaneous Functional Magnetic Resonance Imaging and Electrophysiological Recording”. 《Human Brain Mapping》 3: 13–23. doi:10.1002/hbm.460030103. S2CID 145788101.
- ↑ Goldman, Robin; Stern, John; Engel, John; Cohen, Mark (2000). “Acquiring Simultaneous EEG and Functional MRI”. 《Clinical Neurophysiology》 111 (11): 1974–80. doi:10.1016/s1388-2457(00)00456-9. PMID 11068232. S2CID 11716369.
- ↑ Horovitz, Silvina G.; Skudlarski, Pawel; Gore, John C. (2002). “Correlations and dissociations between BOLD signal and P300 amplitude in an auditory oddball task: A parametric approach to combining fMRI and ERP”. 《Magnetic Resonance Imaging》 20 (4): 319–25. doi:10.1016/S0730-725X(02)00496-4. PMID 12165350.
- ↑ Laufs, H; Kleinschmidt, A; Beyerle, A; Eger, E; Salek-Haddadi, A; Preibisch, C; Krakow, K (2003). “EEG-correlated fMRI of human alpha activity”. 《NeuroImage》 19 (4): 1463–76. CiteSeerX 10.1.1.586.3056. doi:10.1016/S1053-8119(03)00286-6. PMID 12948703. S2CID 6272011.
- ↑ US patent 7286871, Mark S. Cohen, "Method and apparatus for reducing contamination of an electrical signal", published 2004-05-20
- ↑ Difrancesco, Mark W.; Holland, Scott K.; Szaflarski, Jerzy P. (2008). “Simultaneous EEG/Functional Magnetic Resonance Imaging at 4 Tesla: Correlates of Brain Activity to Spontaneous Alpha Rhythm During Relaxation”. 《Journal of Clinical Neurophysiology》 25 (5): 255–64. doi:10.1097/WNP.0b013e3181879d56. PMC 2662486. PMID 18791470.
- ↑ Huizenga, HM; Van Zuijen, TL; Heslenfeld, DJ; Molenaar, PC (2001). “Simultaneous MEG and EEG source analysis”. 《Physics in Medicine and Biology》 46 (7): 1737–51. Bibcode:2001PMB....46.1737H. CiteSeerX 10.1.1.4.8384. doi:10.1088/0031-9155/46/7/301. PMID 11474922.
- ↑ Aydin Ü, Vorwerk J, Dümpelmann M, Küpper P, Kugel H, Heers M, Wellmer J, Kellinghaus C, Haueisen J, Rampp S, Stefan H, Wolters CH (2015). “Combined EEG/MEG can outperform single modality EEG or MEG source reconstruction in presurgical epilepsy diagnosis”. 《PLOS ONE》 (Review) 10 (3): e0118753. Bibcode:2015PLoSO..1018753A. doi:10.1371/journal.pone.0118753. PMC 4356563. PMID 25761059.
- ↑ Schreckenberger, Mathias; Lange-Asschenfeldt, Christian; Lochmann, Matthias; Mann, Klaus; Siessmeier, Thomas; Buchholz, Hans-Georg; Bartenstein, Peter; Gründer, Gerhard (2004). “The thalamus as the generator and modulator of EEG alpha rhythm: A combined PET/EEG study with lorazepam challenge in humans”. 《NeuroImage》 22 (2): 637–44. doi:10.1016/j.neuroimage.2004.01.047. PMID 15193592. S2CID 31790623.
- ↑ Bird, Jordan J.; Manso, Luis J.; Ekart, Aniko; Faria, Diego R. (September 2018). 《A Study on Mental State Classification using EEG-based Brain-Machine Interface》. Madeira Island, Portugal: 9th international Conference on Intelligent Systems 2018. 2018년 12월 3일에 확인함.
- ↑ Bird, Jordan J.; Ekart, Aniko; Buckingham, Christopher D.; Faria, Diego R. (2019). 《Mental Emotional Sentiment Classification with an EEG-based Brain-Machine Interface》. St Hugh's College, University of Oxford, United Kingdom: The International Conference on Digital Image and Signal Processing (DISP'19). 2018년 12월 3일에 확인함.
- ↑ Vanneste S, Song JJ, De Ridder D (March 2018). “Thalamocortical dysrhythmia detected by machine learning”. 《Nature Communications》 (영어) 9 (1): 1103. Bibcode:2018NatCo...9.1103V. doi:10.1038/s41467-018-02820-0. PMC 5856824. PMID 29549239.
참고 문헌[편집]
- Nunez Paul L., Srinivasan Ramesh (2007). “PDF”. 《Scholarpedia》 2 (2): 1348. Bibcode:2007SchpJ...2.1348N. doi:10.4249/scholarpedia.1348.
- Arns, Martijn; Sterman, Maurice B. (2019). 《Neurofeedback: How it all started》. Nijmegen, The Netherlands: Brainclinics Insights. ISBN 9789083001302.
외부 링크[편집]
- Tanzer Oguz I., (2006) Numerical Modeling in Electro- and Magnetoencephalography, Ph.D. Thesis, Helsinki University of Technology, Finland.
- A tutorial on simulating and estimating EEG sources in Matlab Archived 2016년 3월 7일 - 웨이백 머신
- A tutorial on analysis of ongoing, evoked, and induced neuronal activity: Power spectra, wavelet analysis, and coherence Archived 2018년 11월 7일 - 웨이백 머신
