아세틸콜린에스터레이스 억제제
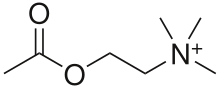

아세틸콜린에스터레이스 억제제(acetylcholinesterase inhibitors, AChEIs, 종종 콜린에스터레이스 억제제[1])는 신경전달물질인 아세틸콜린을 콜린과 아세트산으로 가수분해시키는 효소인 아세틸콜린에스터레이스를 억제하는 약물이다.[2] 따라서 아세틸콜린의 농도와 작용 시간이 아세틸콜린 수용체가 풍부한 중추신경계, 자율신경절, 신경근 접합부에서 증가한다.[2] 아세틸콜린에스터레이스 억제제는 콜린에스터레이스 억제제의 일종으로, 콜린에스터레이스 억제제는 아세틸콜린에스터레이스 억제제와 부티릴콜린에스터레이스 억제제로 나뉜다.[2] 아세틸콜린에스터레이스는 콜린에스터레이스 효소족의 주요 구성원이다.[3]
아세틸콜린에스테레이스 억제제는 가역적(reversible), 비가역적(irreversible), 준가역적(quasi-irreversible 또는 pseudo-irreversible) 억제제로 분류된다.[4][5]
작용 기전[편집]
유기인산화합물[편집]
피로인산 테트라에틸(TEPP)이나 사린과 같은 유기인산화합물은 신경전달물질인 아세틸콜린을 가수분해시키는 콜린에스터레이스를 억제한다.
콜린에스터레이스의 활성 중심에는 음이온 부위(anionic site)와 에스터 부위(esteraic site)라는 두 개의 중요한 부위가 존재한다. 아세틸콜린이 콜린에스터레이스의 음이온 부위에 결합하면 아세틸콜린의 아세틸기가 에스터 부위에 붙을 수 있게 된다. 에스터 부위에 위치한 주요 아미노산 잔기는 글루탐산, 히스티딘, 세린이다. 이 잔기들이 아세틸콜린의 가수분해를 매개한다.

에스터 부위에서 아세틸콜린은 절단되어 유리된 상태의 콜린 일부와 아세틸화된 콜린에스터레이스가 남게 된다. 아세틸화된 상태의 콜린에스터레이스가 자기 자신을 재생하기 위해서는 가수분해되어야 한다.[6][7]
TEPP와 같은 억제제는 콜린에스터레이스의 에스터 부위에 위치한 세린 잔기를 변형시킨다.

인산화로 인해 아세틸콜린의 아세틸기가 콜린에스터레이스의 에스터 부위에 결합하지 못하게 된다. 아세틸기가 콜린에스터레이스에 결합하지 못하면 아세틸콜린이 분해되지 못하게 된다. 따라서 아세틸콜린이 분해되지 않은 채로 남아 시냅스에 쌓이게 된다. 이로 인해 아세틸콜린 수용체가 계속 활성화되고 TEPP 중독의 급성 증상을 유발한다.[8] TEPP(또는 다른 유기인산화합물)에 의한 콜린에스터레이스의 인산화는 비가역적이다. 이 때문에 콜린에스터레이스는 영구적으로 억제된다.[6][7]
콜린에스터레이스는 다음의 반응식에 따라 비가역적으로 인산화된다.
반응식에서 E는 콜린에스터레이스, PX는 TEPP 분자, E-PX가 가역적으로 인산화된 콜린에스터레이스, k3은 두 번째 단계의 반응속도상수, EP는 인산화된 콜린에스터레이스, X는 TEPP의 남은 기(基)이다.
콜린에스터레이스의 비가역적인 인산화는 두 단계에 걸쳐 일어난다. 첫 번째 단계에서 콜린에스터레이스는 가역적으로 인산화되며 매우 반응이 빠르게 일어난다. 그 후 두 번째 단계에서 콜린에스터레이스는 TEPP와 공유 결합하여 매우 안정한 상태의 복합체를 형성한다. 두 번째 단계는 느린 반응이지만 이 단계 후에는 콜린에스터레이스가 비가역적으로 억제된다.[6]
시간에 의존적인 콜린에스터레이스의 비가역적 억제는 다음의 식으로 나타낼 수 있다.[6]
이 공식에서 E는 남은 효소의 활성, E0는 초기 효소의 활성, t는 콜린에스터레이스와 TEPP를 섞은 후의 시간 간격, KI는 콜린에스터레이스-TEPP 복합체(E-PX)의 해리상수, I는 TEPP의 농도를 뜻한다.
위의 반응 기전과 공식은 다른 유기인산화합물에서도 동일하며, 반응 과정 역시 똑같이 일어난다.
더 나아가 특정 유기인산화합물은 유기인산 유도 지연성 다발신경병증(organophosphate-induced delayed polyneuropathy, OPIDN)을 일으킬 수 있다. 이 질환은 말초신경계와 중추신경계의 축삭이 퇴행하는 것이 특징이며, 유기인산에 오염된 이후 수 주 후에 발병한다. 신경병증 표적 에스터레이스(neuropathy target esterase, NTE)이 병의 원인인 유기인산화합물에 의해 영향을 받는 것으로 여겨진다. 그러나 TEPP가 OPIDN을 일으키는 유기인산이라는 근거는 없다.[9]
활용[편집]
아세틸콜린에스터레이스 억제제가 사용되는 곳은 다음과 같다.[6]
- 각종 생물의 독에서 자연적으로 발생하는 경우 (온키달 등)
- 신경독과 같이 무기로 사용되는 경우
- 의료용으로 사용되는 경우
- 중증 근무력증에서 신경근 간의 신호 전달을 증가시키기 위해 치료 목적으로 사용하는 경우
- 녹내장 치료
- 기립성 빈맥 증후군 치료
- 항콜린제 중독에 대한 해독제
- 비탈분극성 근이완제의 효과를 반전시키기 위한 목적
- 알츠하이머병 같은 질병의 신경정신적 증상(특히 무감정)을 치료하기 위한 목적
- 렘수면을 연장시켜 자각몽 발생 확률을 올리기 위한 목적[10]
- 루이체 치매나 파킨슨병, 알츠하이머병 치료 목적. 이러한 신경퇴행성질환에서 AChEI는 주로 치매의 인지적 증상(대부분 기억과 학습 기능 장애)을 치료하기 위해 사용된다. 이러한 증상들은 중추신경계에 작용하는 아세틸콜린의 기능이 줄어드는 것이 원인이 된다. AChEI가 파킨슨병에서 정신적 증상(특히 환시)을 완화시킬 수 있다고 주장하는 근거들도 있다.[11]
- 조현병이 있는 환자의 인지장애를 치료하는 목적. 양성 증후, 음성 증후, 기분장애를 치료하는 데에 AChEI가 효능이 있다는 근거들이 있다.[12][13][14]
- 자폐를 치료하고 자폐가 있는 아동에서 렘수면 비율을 늘리기 위한 목적. 이때는 자각몽을 유발시킬 때와 똑같은 과정이 일어난다.[15][16]
- 살충제로 사용되는 경우 (말라티온 등)
부작용[편집]
| 아세틸콜린에스터레이스 억제제 복용 시 일어날 수 있는 부작용[17][18] | |||
|---|---|---|---|
| 가벼운 부작용 - 보통 사라짐 | 심각할 수 있는 부작용 | ||
콜린에스터레이스 억제제의 주된 효과는 다음과 같다.
- 부교감신경계에 작용하여 서맥, 저혈압, 과다분비, 기관지수축, 위장관계의 운동성 과다(설사), 안압 감소, 아래식도조임근의 근긴장도 증가 등을 일으킬 수 있다.
- 콜린성 위기.
- 신경근 접합부에 작용하며 근수축 시간을 늘릴 수 있다.[19]
- 네오스티그민이 수술 이후의 구역질이나 구토에 미치는 효과에는 논쟁이 있으며 명확한 연결고리가 있지는 않지만, 항콜린제를 처방했을 때 그 위험이 감소한다는 근거는 존재한다.[20]
요폐 환자에서 가역적 콜린에스터레이스 억제제를 복용하는 것은 금기시된다.
과다 복용[편집]
- 니코틴성 아세틸콜린 수용체, 무스카린성 아세틸콜린 수용체의 과도한 자극을 일으킬 수 있다.[4]
목록[편집]
가역적 억제제[편집]
콜린에스터레이스의 가역적 억제제로 작용하는 물질들은 대부분 치료 목적으로 사용되며 다음과 같은 물질들이 있다.
- 아래의 다른 문단에 포함되지 않은 일부 유기인산화합물
- 카바메이트
- 페난트렌 유도체
- 카페인 – 아세틸콜린에스터레이스 비경쟁적 저해제이자 아데노신 수용체 길항제[21]
- 로스마린산 – 카페산의 에스터. 꿀풀과(Lamiaceae)에 속하는 식물 종에서 발견된다.[22]
- 알파 피넨 – 비경쟁적, 가역적 억제제[23][24]
- 피페리딘
- 타크린(테트라하이드로아미노아크리딘, THA')
- 에드로포니움
- 휴페르진 A[25][26]
- 라도스티길
- 은제레마인[27]
- 락토쿠피크린
- 아코티아마이드
비교 표[편집]
| 억제제 | 작용 시간 | 주된 작용 부위 | 임상적 사용 | 부작용 |
|---|---|---|---|---|
| 에드로포니움 | 짧음 (10분) | 신경근 접합부 | 중증 근무력증의 진단 | |
| 네오스티그민 | 중간 (1–2시간) | 신경근 접합부 | 내장 | |
| 피소스티그민 | 중간 (0.5–5시간) | 신경절 이후 부교감신경 | 녹내장 치료 (안약) | |
| 피리도스티그민 | 중간 (2–3시간) | 신경근 접합부 | ||
| 다이아이소프로필 플루오로인산 | 긺 | 신경절 이후 부교감신경 | 역사적으로 녹내장 치료에 이용 (안약) | 독성 |
| 에코티오페이트 (비가역적) | 긺 | 신경절 이후 부교감신경 | 녹내장 치료 (안약) | 전신성 부작용 |
| 파라티온 (비가역적) | 긺 | - | 독성 |
준가역적 억제제[편집]
콜린에스터레이스에 대한 준가역적 억제제로 작용하는 물질들은 농약, 화학무기로 사용되는 경우가 많다.
참고 문헌[편집]
- ↑ “Medications for treating people with dementia” (PDF). 2021년 1월 1일에 확인함.
- ↑ 가 나 다 English, Brett A.; Webster, Andrew A. (2012). 〈Acetylcholinesterase and its Inhibitors〉. 《Primer on the Autonomic Nervous System》. Elsevier. 631–633쪽. doi:10.1016/b978-0-12-386525-0.00132-3. ISBN 978-0-12-386525-0.
- ↑ Seth (2009년 11월 18일). 〈23〉. 《Textbook Of Pharmacology》. Elsevier India. III.87쪽. ISBN 978-8131211588. 2019년 6월 18일에 확인함.
Anaesthesia: Cholinesterase inhibitors are likely to exaggerate succinylcholine-type muscle relaxation during anaesthesia. 5. Genitourinary system: It may ...
- ↑ 가 나 Colović MB, Krstić DZ, Lazarević-Pašti TD, Bondžić AM, Vasić VM (May 2013). “Acetylcholinesterase inhibitors: pharmacology and toxicology”. 《Current Neuropharmacology》 (Bentham Science Publishers Ltd.) 11 (3): 315–35. doi:10.2174/1570159x11311030006. PMC 3648782. PMID 24179466.
- ↑ McGleenon BM, Dynan KB, Passmore AP (October 1999). “Acetylcholinesterase inhibitors in Alzheimer's disease”. 《British Journal of Clinical Pharmacology》 48 (4): 471–80. doi:10.1046/j.1365-2125.1999.00026.x. PMC 2014378. PMID 10583015.
- ↑ 가 나 다 라 마 바 사 Colović MB, Krstić DZ, Lazarević-Pašti TD, Bondžić AM, Vasić VM (May 2013). “Acetylcholinesterase inhibitors: pharmacology and toxicology”. 《Current Neuropharmacology》 11 (3): 315–35. doi:10.2174/1570159X11311030006. PMC 3648782. PMID 24179466.
- ↑ 가 나 O'Brien, Richard D. (2013년 10월 22일). 《Toxic Phosphorus Esters: Chemistry, Metabolism, and Biological Effects》 (영어). Elsevier. ISBN 978-1-4832-7093-7.
- ↑ Roberts, Stephen M.; James, Robert C.; Williams, Phillip L. (2014년 12월 8일). 《Principles of Toxicology: Environmental and Industrial Applications》 (영어). John Wiley & Sons. ISBN 978-1-118-98248-8.
- ↑ Lotti M, Moretto A (2005년 1월 1일). “Organophosphate-induced delayed polyneuropathy”. 《Toxicological Reviews》 24 (1): 37–49. doi:10.2165/00139709-200524010-00003. PMID 16042503. S2CID 29313644.
- ↑ Yuschak, Thomas (2006). 《Advanced Lucid Dreaming: The Power of Supplements》. Lulu. ISBN 978-1430305422.
- ↑ Taylor D, Paton C, Shitij K (2012). 《Maudsley Prescribing Guidelines in Psychiatry》 11판. West Sussex: Wiley-Blackwell. ISBN 978-0-47-097948-8.
- ↑ Singh J, Kour K, Jayaram MB (January 2012). “Acetylcholinesterase inhibitors for schizophrenia”. 《The Cochrane Database of Systematic Reviews》 1: CD007967. doi:10.1002/14651858.CD007967.pub2. PMC 6823258. PMID 22258978.
요약본 - Singh J, Kour K, Jayaram MB. “Acetylcholinesterase inhibitors versus antipsychotics for schizophrenia either alone or in combination with antipsychotics”. 《Cochrane》. - ↑ Choi KH, Wykes T, Kurtz MM (September 2013). “Adjunctive pharmacotherapy for cognitive deficits in schizophrenia: meta-analytical investigation of efficacy”. 《The British Journal of Psychiatry》 203 (3): 172–8. doi:10.1192/bjp.bp.111.107359. PMC 3759029. PMID 23999481.
- ↑ Ribeiz SR, Bassitt DP, Arrais JA, Avila R, Steffens DC, Bottino CM (April 2010). “Cholinesterase inhibitors as adjunctive therapy in patients with schizophrenia and schizoaffective disorder: a review and meta-analysis of the literature”. 《CNS Drugs》 24 (4): 303–17. doi:10.2165/11530260-000000000-00000. PMID 20297855. S2CID 45807136.
- ↑ Buckley AW, Sassower K, Rodriguez AJ, Jennison K, Wingert K, Buckley J, Thurm A, Sato S, Swedo S (August 2011). “An open label trial of donepezil for enhancement of rapid eye movement sleep in young children with autism spectrum disorders”. 《Journal of Child and Adolescent Psychopharmacology》 21 (4): 353–7. doi:10.1089/cap.2010.0121. PMC 3157749. PMID 21851192.
- ↑ Handen BL, Johnson CR, McAuliffe-Bellin S, Murray PJ, Hardan AY (February 2011). “Safety and efficacy of donepezil in children and adolescents with autism: neuropsychological measures”. 《Journal of Child and Adolescent Psychopharmacology》 21 (1): 43–50. doi:10.1089/cap.2010.0024. PMC 3037196. PMID 21309696.
- ↑ Consumer Reports; Drug Effectiveness Review Project (May 2012). “Evaluating Prescription Drugs Used to Treat: Alzheimer's Disease Comparing Effectiveness, Safety, and Price” (PDF). 《Best Buy Drugs》: 2. 2012년 9월 5일에 원본 문서 (PDF)에서 보존된 문서. 2013년 5월 1일에 확인함., which claims Alzheimer's Association guidance as a source
- ↑ Inglis F (June 2002). “The tolerability and safety of cholinesterase inhibitors in the treatment of dementia”. 《International Journal of Clinical Practice. Supplement》 (127): 45–63. PMID 12139367.
- ↑ Singh, Ravneet; Sadiq, Nazia M. (2020), “Cholinesterase Inhibitors”, 《StatPearls》 (Treasure Island (FL): StatPearls Publishing), PMID 31335056, 2020년 10월 12일에 확인함
- ↑ Barash, Paul G; Cullen, Bruce F; Stoelting, Robert K; Cahalan, Michael K; Stock, M Christine (2013년 4월 15일). 《Clinical Anesthesia》 7판. 552–554쪽. ISBN 978-1-4511-4419-2.
- ↑ Karadsheh N, Kussie P, Linthicum DS (March 1991). “Inhibition of acetylcholinesterase by caffeine, anabasine, methyl pyrrolidine and their derivatives”. 《Toxicology Letters》 55 (3): 335–42. doi:10.1016/0378-4274(91)90015-X. PMID 2003276.
- ↑ Vladimir-Knežević S, Blažeković B, Kindl M, Vladić J, Lower-Nedza AD, Brantner AH (January 2014). “Acetylcholinesterase inhibitory, antioxidant and phytochemical properties of selected medicinal plants of the Lamiaceae family”. 《Molecules》 19 (1): 767–82. doi:10.3390/molecules19010767. PMC 6271370. PMID 24413832.
- ↑ Miyazawa M, Yamafuji C (March 2005). “Inhibition of acetylcholinesterase activity by bicyclic monoterpenoids”. 《Journal of Agricultural and Food Chemistry》 53 (5): 1765–8. doi:10.1021/jf040019b. PMID 15740071.
- ↑ Perry NS, Houghton PJ, Theobald A, Jenner P, Perry EK (July 2000). “In-vitro inhibition of human erythrocyte acetylcholinesterase by salvia lavandulaefolia essential oil and constituent terpenes”. 《The Journal of Pharmacy and Pharmacology》 52 (7): 895–902. doi:10.1211/0022357001774598. PMID 10933142. S2CID 34457692.
- ↑ Bauer, Brent A. “Huperzine A: Can it treat Alzheimer's?”. 《Mayo Clinic》. 2012년 8월 19일에 원본 문서에서 보존된 문서.
- ↑ Wang BS, Wang H, Wei ZH, Song YY, Zhang L, Chen HZ (April 2009). “Efficacy and safety of natural acetylcholinesterase inhibitor huperzine A in the treatment of Alzheimer's disease: an updated meta-analysis”. 《Journal of Neural Transmission》 116 (4): 457–65. doi:10.1007/s00702-009-0189-x. PMID 19221692. S2CID 8655284.
- ↑ Rhee IK, Appels N, Hofte B, Karabatak B, Erkelens C, Stark LM, Flippin LA, Verpoorte R (November 2004). “Isolation of the acetylcholinesterase inhibitor ungeremine from Nerine bowdenii by preparative HPLC coupled on-line to a flow assay system”. 《Biological & Pharmaceutical Bulletin》 27 (11): 1804–9. doi:10.1248/bpb.27.1804. PMID 15516727.
- ↑ Rang HP (2003). 《Pharmacology》. Edinburgh: Churchill Livingstone. 156쪽. ISBN 978-0-443-07145-4.
외부 링크[편집]
- 의학주제표목 (MeSH)의 Acetylcholinesterase+inhibitors
- Acetylcholinesterase: A gorge-ous enzyme QUite Interesting PDB Structure article at PDBe

![{\displaystyle {\ce {E + PX <=> E-PX ->[k_3] EP + X}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/896525e22a1d1b440d2154f6a1cde9e1ddbef67d)
