과산화 칼륨

| |
| 이름 | |
|---|---|
| IUPAC 이름
Potassium peroxide
| |
| 식별자 | |
3D 모델 (JSmol)
|
|
| ChemSpider | |
| ECHA InfoCard | 100.037.339 |
| EC 번호 |
|
PubChem CID
|
|
| UNII | |
CompTox Dashboard (EPA)
|
|
| |
| |
| 성질 | |
| K2O2 | |
| 몰 질량 | 110.196 g/mol |
| 겉보기 | yellow amorphous solid |
| 녹는점 | 490 °C (914 °F; 763 K) |
| 물과 반응[1] | |
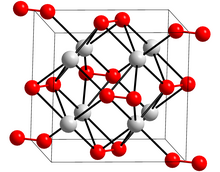
| 구조 | |
| 사방정계 | |
| Cmca, oS16 | |
| 열화학 | |
표준 몰 엔트로피 (S
|
113 J·mol−1·K−1[2] |
표준 생성 엔탈피 (ΔfH⦵298)
|
−496 kJ·mol−1[2] |
| 위험 | |
| NFPA 704 (파이어 다이아몬드) | |
| 관련 화합물 | |
다른 음이온
|
산화 칼륨 en:Potassium superoxide 염화 칼륨 |
다른 양이온
|
과산화 리튬 en:Sodium peroxide |
달리 명시된 경우를 제외하면, 표준상태(25 °C [77 °F], 100 kPa)에서 물질의 정보가 제공됨.
| |
과산화 칼륨(過酸化─, potassium peroxide)은 화학식 K2O2를 갖는 무기 화합물이다.
산화 칼륨(K2O), 초산화 칼륨(KO2)과 더불어 칼륨이 대기 중 산소와 반응하면서 형성된다.
과산화 칼륨은 물과 반응하면 수산화 칼륨과 산소를 만들어낸다:
각주[편집]
- ↑ Lide, David R. (1998). 《Handbook of Chemistry and Physics》 87판. Boca Raton, Florida: CRC Press. 477; 520쪽. ISBN 0-8493-0594-2.
- ↑ 가 나 Zumdahl, Steven S. (2009). 《Chemical Principles 6th Ed.》. Houghton Mifflin Company. A22쪽. ISBN 978-0-618-94690-7.


