미토콘드리아 DNA
미토콘드리아 DNA(영어: mitochondrial DNA, mtDNA 또는 mDNA)[2]는 세포소기관인 미토콘드리아에 존재하는 DNA이다. 미토콘드리아 DNA는 진핵세포에 있는 DNA 중 극히 일부를 차지한다. 대부분의 DNA는 핵 내에 존재하며, 식물의 경우에는 핵과 엽록체에 존재한다.
사람 미토콘드리아 DNA는 가장 작은 염색체로 간주하며, 37개 유전자와 약 16,600개 염기쌍이 있다. 사람 미토콘드리아 DNA는 사람 유전체 가운데 처음으로 서열을 밝혔다. 사람을 포함한 대부분 종에서 미토콘드리아 DNA는 오직 모계로만 유전된다.[3]
몇몇 멸종된 생물을 포함하여 다수의 생물과 개인의 미토콘드리아 DNA의 서열이 밝혀져 있다. 멸종된 생물의 DNA 서열은 종 사이의 진화적 관계를 밝히는 데 사용되며 계통학의 근간이 된다. 미토콘드리아 DNA는 또한 인류학과 생태학에서는 인종 간의 관계를 밝히는 데 쓰인다.
기원[편집]
핵 DNA와 미토콘드리아 DNA는 진화적으로 서로 다른 기원을 가지고 있는 것으로 알려져 있다. 미토콘드리아 DNA는 오늘날 진핵세포의 초기 조상에게 잡아먹힌(engulfed) 박테리아의 원형 DNA에서 유래했을 것으로 추정된다. 이 이론은 세포 내 공생설이라고 한다. 각 미토콘드리아는 약 2-10개의 미토콘드리아 DNA 복사본을 가지고 있다.[4] 현존하는 세포의 미토콘드리아 단백질은 거의 대부분이 핵 DNA에 암호화되어 있으며, 이들 핵 DNA는 박테리아에서 기원하여 진화하는 동안 진핵생물의 핵으로 옮겨갔을 것으로 추정된다.[5]포유류의 경우 미토콘드리아 단백질 1500여 종류가 핵 DNA에 암호화되어 있다.
구조[편집]
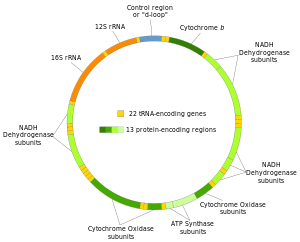
다세포생물의 미토콘드리아 DNA는 대부분 공유결합으로 닫힌 원형 이중가닥 DNA이다. 단세포생물(e.g. 섬모충인 테트라하이메나 혹은 녹조류인 Chlamydomonas reinhardtii)과 드물게 다세포생물(e.g. 자포동물 중 몇몇 종)의 경우 미토콘드리아 DNA가 선형이다. 이런 선형 DNA는 텔로머레이스에 독립적인 텔로미어를 가지고 있으며 특수한 방법으로 복제된다. 선형 미토콘드리아 DNA를 가진 단세포생물 중에는 병원체가 많아 사람의 원형 미토콘드리아 DNA는 교란시키지 않고 병원체만 교란시키는 약물의 표적이 된다.[6]
일반적으로 사람을 포함한 후생동물 세포 한 개당 미토콘드리아 DNA 100-10,000개 복사본이 있다.[주 1] 포유류의 경우 각 이중가닥 원형 미토콘드리아 DNA 분자는 15,000-17,000개[7]의 염기쌍으로 이루어진다. 미토콘드리아 DNA의 양쪽 가닥은 뉴클레오타이드 함량이 다르다. 구아닌이 풍부한 가닥은 무거운 사슬(heavy strand, H-strand)로, 시토신이 풍부한 가닥은 가벼운 사슬(L-strand)로 불린다. 무거운 사슬에는 28개, 가벼운 사슬에는 9개의 유전자가 암호화되어 있다. 총 37개의 유전자 중 13개는 단백질(폴리펩티드)로 발현되고, 22개는 전령 RNA(tRNA), 그리고 나머지 2개는 리보솜 RNA(rRNA)의 대단위 및 소단위가 된다. 몇몇 종은 유전자 한두 개가 부족하고 미토콘드리아 DNA의 크기가 큰 경우도 있지만, 이 비율은 대부분의 후생동물에서 일정하다. 진균류와 식물은 유전자의 수와 DNA의 크기에서 훨씬 큰 차이를 보이고, 이 경우에도 진핵생물에 존재하는 주요 유전자는 모두 가지고 있다. 특정 식물 종은 염기쌍 2,500,000개에 달하는 미토콘드리아 DNA를 가지고 있기도 하지만 훨씬 적은 양의 미토콘드리아 DNA를 가진 유사한 종과 유전자 수와 종류는 같다.[8]
복제[편집]
미토콘드리아 DNA는 DNA 중합효소 γ복합체로 복제된다. DNA 중합효소 γ복합체는 POLG에 암호화된 140 kDa의 DNA 중합효소와 POLG2에 암호화된 55 kDa의 부가적인 소단위로 이루어진다.[9] 복제 기구는 DNA 중합효소, TWINKLE 그리고 미토콘드리아 단백질 SSB 단백질로 이루어진다. TWINKLE은 헬리케이스로 이중가닥 DNA(dsDNA)의 일부분을 5'에서 3' 방향으로 풀어준다.[10]
수정 후 착상 전까지 미토콘드리아 DNA의 복제는 억제된다.[9] 배반포 단계에서 영양외배엽의 세포들에서는 미토콘드리아 DNA의 복제가 시작되지만, 내세포괴의 세포들은 특정한 세포로 분화되는 신호를 받을 때까지 미토콘드리아 DNA의 복제가 시작되지 않는다.[9]
미토콘드리아 유전[편집]
대부분의 다세포생물의 경우 미토콘드리아 DNA는 어머니를 통해서 유전된다. 정자가 100-1,000개의 미토콘드리아 DNA 분자를 가지고 있는 반면, 난자는 100,000-1,000,000개의 분자를 갖는다. 일반적으로 동물의 예에서 수컷의 정자와 암컷의 난자가 수정될 때 정자의 미토콘드리아 DNA는 참여하지 못하며, 수정란에 있는 모계의 미토콘드리아 DNA은 다른 미토콘드리아와 재조합하지 않는다고 이해되고 있어 모계에서 모계로의 유래된 미토콘드리아DNA의 비율이 유지된다고 보고있다.[11]
모계 유전[편집]
유성생식하는 생물은 미토콘드리아를 모계로부터 받는다. 포유류의 정자에 있는 미토콘드리아는 수정 후 난세포에 의해 파괴된다.[12] 또한 정자의 미토콘드리아는 추진력을 얻기 위해 꼬리에 있으며, 수정 중에 꼬리는 떨어져 나간다. 부계 미토콘드리아 DNA를 가진 미토콘드리아는 배아 내에서 유비퀴틴으로 표지된다는 보고가 있다.[13] 시험관 수정 기술, 특히 정자를 난세포에 주입하는 인공수정 기술은 이 과정을 방해할 수 있다.
미토콘드리아 DNA가 모계 유전된다는 사실을 이용하여 유전계보학자들은 모계 사회를 추적한다.[주 2] 미토콘드리아 DNA에 있는 고도가변 조절영역(hypervariable control region, HVR)의 서열을 파악하여 DNA 계보 실험(genealogical DNA test)을 한다. HVR1은 약 440개의 염기쌍으로 이루어져 있는데, 이 염기쌍을 데이터베이스나 대상의 HVR과 비교하여 모계 계보를 결정한다.[14] 미토콘드리아 이브도 같은 유형의 분석을 통해 인류의 기원으로 추정되고 있다.
미토콘드리아 DNA는 빨리 돌연변이를 일으키고 잘 보존되어 있지 않기 때문에 진화적 관계를 파악하는데 유용하다. 서로 다른 종들 간에 미토콘드리아 DNA를 비교하여 계통수를 작성한다.
부계 유전[편집]
몇몇 홍합(mussel) 종은 때로 부계 미토콘드리아 DNA가 전달되기도 한다.[15][16] 미토콘드리아가 부계 유전되는 사례에는 초파리,[17] 꿀벌,[18] 그리고 매미[19] 도 포함된다. 부계 유전 사례는 드물게 포유류에서 발견되기도 한다. 쥐에서 그러한 사례가 보고된 바 있지만, 결과적으로는 수컷에서 유래한 미토콘드리아는 제거되었다.[20][21] 양[22]과 복제 소에서도 보고된 사례가 있다.[23] 사람의 경우 보고된 사례가 한 개 있는데, 대상은 남자였다.[24]
돌연변이[편집]

취약성[편집]
미토콘드리아에는 호흡 사슬이 있으므로 미토콘드리아 DNA는 활성산소에 특히 취약하다. 미토콘드리아 DNA는 단백질로 싸여 있고 DNA 수리 기구를 가지고 있지만, 핵 DNA의 그것들만큼 성능이 뛰어나지는 않다. 따라서 미토콘드리아 DNA에 산화적 손상으로 돌연변이가 생길 수 있고, 그 결과 단백질을 암호화하는 서열이 변하여 생명체의 대사나 건강에 영향을 미칠 수 있다.[25]
유전 질환[편집]
미토콘드리아 DNA 돌연변이로 생기는 질병에는 운동불내성과 심장, 눈, 근육 운동 기능을 잃는 병인 컨즈-세이어 증후군(Kearns-Sayre syndrome, KSS) 등이 있다. 노화 및 노화와 관련된 질병의 주요 원인이 미토콘드리아 DNA라는 증거가 있다.[26]
진단에 사용[편집]
미토콘드리아 DNA 삭제 돌연변이는 생검 결과 음성인 전립선암을 진단하는 데 도움이 되었다.[27][28]
노화와의 관계[편집]
노화와 미토콘드리아 DNA의 상관성에는 아직 논란의 여지가 있다. 노화가 미토콘드리아 유전체에 기능 장애를 일으킨다는 보고가 있다.[29] 미토콘드리아 DNA에 돌연변이가 생기면 활성산소 생산과 활성산소를 제거하는 효소(e.g. 과산화물 제거효소, 카탈레이스, 글루타티온 과산화효소 등) 사이의 균형이 흔들린다. 활성산소에 의하여 미토콘드리아 DNA에 유전적 손상이 축적되면 미토콘드리아는 기능을 상실하고 자유 라디칼을 세포질로 방출한다. 또한 미토콘드리아의 기능이 떨어지면 전체 대사 효율이 감소한다.[30] 미토콘드리아 DNA의 생화학적 특성과 그 종의 수명 사이에 상관관계가 있음을 보여주는 연구 결과도 있다.[31] 노화 연구를 위한 실마리와 연구 방법을 찾기 위해 다양한 연구가 진행되고 있다.[32][33]
개인 식별에 사용[편집]
핵 DNA는 양쪽 부모로부터 받고, 유전자는 재조합을 통해 재배열된다. 하지만 미토콘드리아 DNA는 대개 부모에서 자식으로 아무런 변화 없이 전해진다. 미토콘드리아 DNA도 재조합이 일어나기는 하지만 같은 미토콘드리온[주 3] 내의 스스로의 복제본끼리만 일어난다. 이러한 이유에 미토콘드리아 DNA의 돌연변이율이 높은 것이 더해져[34] 미토콘드리아 DNA는 모계 조상을 추적하는 강력한 도구가 되었다. 미토콘드리아 DNA는 다양한 종의 수백 세대 이전 조상까지 추적하는데 쓰였다.
미토콘드리아 DNA는 유효 집단의 크기가 작고 돌연변이율이 높아서 동일 종 내에서 개인이나 집단의 유전적 연관성을 파악하고 종들 간에 계통을 확인하는데 유용한 도구가 되었다. 생물학자들은 미토콘드리아 DNA 서열을 파악하고 비교하여 자료를 얻고 서열 간의 관계도, 곧 생물들 간의 관계도를 작성한다. 서열의 유사도를 파악하는 방법은 미토콘드리아 DNA에 생기는 돌연변이로 인하여 한계가 있다. 두 종이 가까운 편에 속할 때는 미토콘드리아 DNA 서열에서 차이나는 부분을 셀 수 있으므로 매우 유용하지만, 종 사이가 멀어지면서 서열 간의 차이가 커지면 세는 것이 불가능해진다.
1996년 미국 테네시 주와 폴 웨어(Paul Ware) 재판에서 최초로 미토콘드리아 DNA를 법의학적 증거로 채택하였다.[35] 2002년 캘리포니아 주에서 있었던 재판에서는 사람과 개의 신원 확인에 사용되었으며,[36] 이것은 미국에서 개의 DNA를 증거로 채택한 최초의 사례가 되었다.[37]
한국에서는 2006년 서울 서초동 서래마을 영아유기 사건에서 모계 감별에 사용된 바 있다.[38][39]
역사[편집]
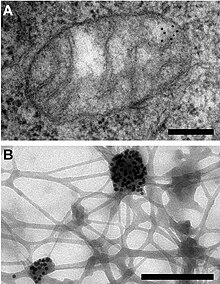
1960년대에 마짓 M. K. 나스(Margit M. K. Nass)와 실반 나스(Sylvan Nass)가 전자현미경을 이용하여 DNA 분해효소에 취약하고 실처럼 생긴 구조물을 미토콘드리아에서 발견하였다.[40]
같이 보기[편집]
- 하플로그룹
- 인류 미토콘드리아 DNA 하플로그룹
- 미토콘드리아 이브
- en:Human mitochondrial genetics
- en:Mitochondrial disease
- en:Paternal mtDNA transmission
각주[편집]
- 내용주
- 참조주
- ↑ Iborra, Francisco J.; Kimura, Hiroshi; Cook, Peter R. (2004). “The functional organization of mitochondrial genomes in human cells”. BMC Biol. (영어) 2: 9. doi:10.1186/1741-7007-2-9. PMID 15157274.
- ↑ Sykes, Bryan (2003년 9월 10일). “Mitochondrial DNA and human history”. The Human Genome (영어). Wellcome Trust. 2015년 9월 7일에 원본 문서에서 보존된 문서. 2014년 7월 9일에 확인함.
- ↑ “Mitochondrial DNA: The Eve Gene”. Bradshaw Foundation (영어). Bradshaw Foundation. 2013년 7월 12일에 원본 문서에서 보존된 문서. 2012년 11월 5일에 확인함.
- ↑ Wiesner RJ, Ruegg JC, Morano I (1992). “Counting target molecules by exponential polymerase chain reaction, copy number of mitochondrial DNA in rat tissues”. 《Biochim Biophys Acta.》 183 (2): 553–559. doi:10.1016/0006-291X(92)90517-O. PMID 1550563.
- ↑ Lodish H, Berk A, Zipursky SL; 외. (2000). “Section 17.1Synthesis and Targeting of Mitochondrial and Chloroplast Proteins”. Molecular Cell Biology (영어) 4판. New York: W. H. Freeman.
- ↑ Nosek J, Tomáska L, Fukuhara H, Suyama Y, Kovác L (1998년 5월). “Linear mitochondrial genomes: 30 years down the line”. Trends Genet. (영어) 14 (5): 184–8. doi:10.1016/S0168-9525(98)01443-7. PMID 9613202.
- ↑ “Genetic Genealogy” (영어). Ramsdale.org. 2003년 5월 19일. 2014년 7월 10일에 확인함.
- ↑ Ward BL, Anderson RS, Bendich AJ (1981년 9월). “The mitochondrial genome is large and variable in a family of plants (cucurbitaceae)”. Cell (영어) 25 (3): 793–803. doi:10.1016/0092-8674(81)90187-2. PMID 6269758. 2010년 8월 9일에 확인함.
- ↑ 가 나 다 John JC, Facucho-Oliveira J, Jiang Y, Kelly R, Salah R (2010년 3월). “Mitochondrial DNA transmission, replication and inheritance: a journey from the gamete through the embryo and into offspring and embryonic stem cells”. Hum Reprod Update (영어) 16 (5): 488–509. doi:10.1093/humupd/dmq002. PMID 20231166.
- ↑ Jemt E, Farge G, Bäckström S, Holmlund T, Gustafsson CM, Falkenberg M (2011년 11월). “The mitochondrial DNA helicase TWINKLE can assemble on a closed circular template and support initiation of DNA synthesis”. Nucleic Acid Res (영어) 39 (21): 9238–9249. doi:10.1093/nar/gkr653. PMC 3241658. PMID 21840902.
- ↑ [참고](국립생물자원관-미토콘드리아 유전체)https://species.nibr.go.kr/UPLOAD_TOTL//CMS/424/content.htm;jsessionid=nUFXQa1TaOqUFW13wKabCthetBAUTfLzXyr1C2JD7Bx5Ob6RpaaJD1R8KzqQYz0t.totl_was_servlet_engine1
- ↑ Cummins, J. M. (2000). “Fertilization and elimination of the paternal mitochondrial genome” (PDF). Human Reproduction (영어) 15: 92–101. PMID 11041517.
- ↑ Sutovsky, P.; 외. (1999년 11월 25일). “Ubiquitin tag for sperm mitochondria”. Nature (영어) 402 (6760): 371–372. doi:10.1038/46466. PMID 10586873.
- ↑ Vilà C, Savolainen P, Maldonado JE, and Amorin IR (1997년 6월 13일). “Multiple and Ancient Origins of the Domestic Dog”. Science (영어) 276 (5319): 1687–1689. doi:10.1126/science.276.5319.1687. ISSN 0036-8075. PMID 9180076.
- ↑ Hoeh WR, Blakley KH, Brown WM (1991). “Heteroplasmy suggests limited biparental inheritance of Mytilus mitochondrial DNA”. Science (영어) 251 (5000): 1488–1490. doi:10.1126/science.1672472. PMID 1672472.
- ↑ Penman, Danny (2002년 8월 23일). “Mitochondria can be inherited from both parents”. 《NewScientist.com》. 2008년 10월 11일에 원본 문서에서 보존된 문서. 2008년 2월 5일에 확인함.
- ↑ Kondo R, Matsuura ET, Chigusa SI (1992). “Further observation of paternal transmission of Drosophila mitochondrial DNA by PCR selective amplification method,”. Genet. Res. (영어) 59 (2): 81–4. doi:10.1017/S0016672300030287. PMID 1628820.
- ↑ Meusel MS, Moritz RF (1993). “Transfer of paternal mitochondrial DNA during fertilization of honeybee (Apis mellifera L.) eggs”. Curr. Genet. (영어) 24 (6): 539–43. doi:10.1007/BF00351719. PMID 8299176.
- ↑ Fontaine, KM, Cooley, JR, Simon, C (2007). “Evidence for Paternal Leakage in Hybrid Periodical Cicadas (Hemiptera: Magicicada spp.)”. PLoS One. (영어) 9 (9): e892. doi:10.1371/journal.pone.0000892. PMC 1963320. PMID 17849021.
- ↑ Gyllensten U, Wharton D, Josefsson A, Wilson AC (1991). “Paternal inheritance of mitochondrial DNA in mice”. Nature (영어) 352 (6332): 255–7. doi:10.1038/352255a0. PMID 1857422.
- ↑ Shitara H, Hayashi JI, Takahama S, Kaneda H, Yonekawa H (1998). “Maternal inheritance of mouse mtDNA in interspecific hybrids: segregation of the leaked paternal mtDNA followed by the prevention of subsequent paternal leakage”. Genetics (영어) 148 (2): 851–7. PMC 1459812. PMID 9504930.
- ↑ Zhao X, Li N, Guo W; 외. (2004). “Further evidence for paternal inheritance of mitochondrial DNA in the sheep (Ovis aries)”. Heredity (영어) 93 (4): 399–403. doi:10.1038/sj.hdy.6800516. PMID 15266295.
- ↑ Steinborn R, Zakhartchenko V, Jelyazkov J; 외. (1998). “Composition of parental mitochondrial DNA in cloned bovine embryos”. FEBS Lett. (영어) 426 (3): 352–6. doi:10.1016/S0014-5793(98)00350-0. PMID 9600265.
- ↑ Schwartz M, Vissing J (2002). “Paternal inheritance of mitochondrial DNA”. N. Engl. J. Med. (영어) 347 (8): 576–80. doi:10.1056/NEJMoa020350. PMID 12192017.
- ↑ Michael Hogan (2010). E. Monosson, 편집. “Mutation” (영어). Washington DC: Encyclopedia of Earth. National Council for Science and the Environment.
- ↑ Alexeyev MF, Ledoux SP, Wilson GL. (2004년 6월). “Mitochondrial DNA and aging” (PDF). Clinical Science (영어) 107 (4): 355–364. doi:10.1042/CS20040148. PMID 15279618.
- ↑ Reguly B, Jakupciak JP, Parr RL. (2010). “3.4 kb mitochondrial genome deletion serves as a surrogate predictive biomarker for prostate cancer in histopathologically benign biopsy cores”. Journal de l'Association des urologues du Canada (영어) 4 (5): E118–22. PMC 2950771. PMID 20944788.
- ↑ Robinson K, Creed J, Reguly B, Powell C, Wittock R, Klein D, Maggrah A, Klotz L, Parr RL, Dakubo GD. (2010년 6월). “Accurate prediction of repeat prostate biopsy outcomes by a mitochondrial DNA deletion assay”. Prostate Cancer Prostatic Dis. (영어) 13 (2): 126–31. doi:10.1038/pcan.2009.64. PMID 20084081.
- ↑ de Grey, Aubrey. “The Mitochondrial Free Radical Theory of Aging” (PDF) (영어). Pliki.supernova.com.pl. 2013년 10월 19일에 원본 문서 (PDF)에서 보존된 문서. 2014년 7월 10일에 확인함.
- ↑ Mark K. Shigenaga, Tory M. Hagen and Bruce N. Ames (1994년 11월 8일). “Oxidative Damage and Mitochondrial Decay in Aging” (PDF). Proc Natl Acad Sci USA (영어) 91 (23): 10771–10778. 2015년 9월 24일에 원본 문서 (PDF)에서 보존된 문서. 2014년 7월 10일에 확인함.
- ↑ Aledo JC, Li Y, de Magalhaes JP, Ruiz-Camacho M, Perez-Claros JA (2011). “Mitochondrially encoded methionine is inversely related to longevity in mammals”. Aging Cell (영어) 10 (2): 198–207. doi:10.1111/j.1474-9726.2010.00657.x. PMID 21108730.
- ↑ Carlos K. B. Ferrari (2004). “Functional foods, herbs and nutraceuticals: towards biochemical mechanisms of healthy aging”. BIOGERONTOLOGY (영어) 5 (5): 275–289. doi:10.1007/s10522-004-2566-z.
- ↑ Taylor, Robert W (2005년 2월). “Gene therapy for the treatment of mitochondrial DNA disorders.”. Expert Opinion on Biological Therapy (영어) 5 (2): 183–194. PMID 15757380.
- ↑ Brown WM, George M Jr., Wilson AC (1979). “Rapid evolution of animal mitochondrial DNA”. Proc Natl Acad Sci USA (영어) 76 (4): 1967–1971. doi:10.1073/pnas.76.4.1967. PMID 109836.
- ↑ C. Leland Davis (1998). “Mitochondrial DNA: State of Tennessee v. Paul Ware” (PDF) (영어). 2014년 7월 11일에 확인함.
- ↑ Stevenson, C. (2011년 6월 22일). Rush to Judgement: a critical examination of the David Westerfield, Danielle van Dam child kidnapping and murder case, San Diego 2002 (영어). CreateSpace. 281–288쪽. ISBN 1460956974.
- ↑ “Canine DNA Admitted In California Murder Case” (영어). Pit Bulletin Legal News. 2014년 2월 2일에 원본 문서에서 보존된 문서. 2014년 7월 11일에 확인함.
- ↑ 이은정 (2006년 9월). “DNA는 비밀을 알고 있다” (PDF). 한국과학기술단체총연합회(KOFST). 2014년 7월 14일에 원본 문서 (PDF)에서 보존된 문서. 2014년 7월 10일에 확인함.
- ↑ 한면수 (2007년 6월 26일). 김형근, 편집. “서래마을 영아살해 사건”. 《DNA와 과학수사(21)》. 사이언스타임즈. 2014년 7월 10일에 확인함.
- ↑ NASS MM, NASS S (1963년 12월). “INTRAMITOCHONDRIAL FIBERS WITH DNA CHARACTERISTICS : I. Fixation and Electron Staining Reactions” (PDF). The Journal of Cell Biology (영어) 19 (3): 593–611. doi:10.1083/jcb.19.3.593. PMID 14086138.
