에탄올 발효

에탄올 발효(영어: ethanol fermentation) 또는 알코올 발효(영어: alcoholic fermentation)는 포도당, 과당, 그리고 설탕과 같은 당류를 에탄올과 이산화 탄소로 분해하면서 에너지를 방출하는 생물학적 대사 과정이다. 효모는 산소가 없는 상태에서 이러한 대사를 수행하기 때문에, 에탄올 발효는 혐기적인 대사과정으로 간주된다. 또한 에탄올 발효는 금붕어와 잉어와 같은 일부 어류 종에서 일어나며, 산소가 부족할 때 젖산 발효와 함께 에너지를 공급한다.[1]
에탄올 발효는 알코올 음료의 생산, 에탄올 연료의 생산, 제빵 과정 등을 포함하여 많은 용도로 사용된다.
에탄올 발효의 생화학적 과정[편집]


아래의 화학 반응식은 설탕()에서 에탄올()로의 발효 과정을 요약한 것이다. 에탄올 발효는 1분자의 포도당을 2분자의 에탄올과 2분자의 이산화 탄소로 전환시키고, 2분자의 ATP를 생성한다.
알코올 발효의 전체적인 화학 반응식은 다음과 같다.
설탕은 포도당과 과당으로 구성된 이당류이다. 수크레이스는 포도당과 과당 분자 사이의 글리코사이드 결합을 분해한다.
다음으로 포도당 1분자는 해당과정을 통해 2분자의 피루브산으로 분해된다.[2] 해당과정은 다음의 반응식으로 요약된다.
CH3COCOO−는 피루브산이고, Pi는 무기인산이다. 다음 과정에서 피루브산은 에탄올과 CO2로 전환되며, 해당과정에 필요한 산화된 NAD+를 재생성한다.
- 1. CH3COCOO− + H+ → CH3CHO + CO2
위의 반응은 피루브산 탈카복실화효소에 의해 촉매된다.
- 2. CH3CHO + NADH+H+ → C2H5OH + NAD+
반응식에 나타난 바와 같이 해당과정은 2분자의 NAD+를 2분자의 NADH로 환원시킨다. 또한 2분자의 ADP는 기질수준 인산화를 통해 2분자의 ATP와 2분자의 물(H2O)로 전환된다.
관련된 대사 과정[편집]
당이 에탄올과 CO2로 발효되는 것은 Zymomonas mobilis에 의해서도 이루어지지만, 그 대사 경로가 조금 다른데 해당과정에 의해 피루브산이 생성되는 것이 아니라, 엔트너-듀도로프(Entner–Doudoroff) 경로에 의해 피루브산이 생성된다. 다른 미생물들도 당을 에탄올로 발효시킬 수 있지만 종종 부산물로만 생성한다. 예시들은 다음과 같다.[4]
- Leuconostoc 속 세균이 젖산, 에탄올, CO2를 생성하는 이형젖산 발효(heterolactic acid fermentation)
- 대장균속(Escherichia) 세균이 젖산, 아세트산, 석신산, 포름산, CO2, H2와 혼합된 에탄올을 생성하는 혼합 유기산 발효(mixed acid fermentation)
- Enterobacter 속 세균이 에탄올, 뷰테인다이올(부탄디올), 젖산, 포름산, CO2, H2를 생성하는 뷰테인다이올 발효(butanediol fermentation)
갤러리[편집]
-
포도주 생산 과정에서 발효되는 포도
-
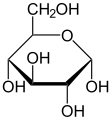
하워드 투영식으로 나타낸 포도당
산소의 효과[편집]
발효는 산소를 필요로 하지 않는다. 산소가 존재하면 일부 효모 종(예: Kluyveromyces lactis 또는 Kluyveromyces lipolytica)은 세포 호흡을 통해 피루브산을 이산화 탄소(CO2)와 물(H2O)로 완전히 산화시키기 때문에, 이러한 효모 종들은 혐기성 환경(세포 호흡이 아닌)에서만 에탄올을 생성한다.
그러나 일반적으로 사용되는 빵효모인 Saccharomyces cerevisiae 또는 분열효모인 Schizosaccharomyces pombe 와 같은 많은 효모들은 세포 호흡보다 발효를 더 선호한다. 이러한 효모들은 적절한 종류의 영양이 제공된다면 호기성 조건하에서도 에탄올을 생산한다. 비연속 발효 중에 세포 단백질 1mg당 에탄올의 생성 속도는 반응 초기의 짧은 시간 동안 극대화되며, 배지에 에탄올이 축적됨에 따라 속도는 점진적으로 감소한다. 이러한 연구는 축적된 에탄올의 제거가 즉각적으로 발효 활성을 회복시키지 못함을 보여주며, 대사 속도의 감소는 에탄올의 존재보다는 생리적인 변화(에탄올에 의한 손상 가능성을 포함하는)때문이라는 증거를 제시한다. 발효 활성의 감소에 대한 몇 가지 잠재적인 원인이 조사되었다. 생존 능력은 90% 이상으로 유지되었고, 내부 pH는 중성에 가깝고, 생체 외에서 측정된 해당과정 효소와 알코올 생성 효소들의 비활성(specific activity)은 비연속 발효 동안 높게 유지되었다. 이러한 요인들 중 어떤 것도 비연속 발효 중 발효 활성의 감소와 관련이 있는 것으로 보이지 않는다.
제빵[편집]

에탄올 발효는 빵 반죽을 부풀게 한다. 효모는 반죽에서 설탕을 소비하고, 에탄올과 이산화 탄소를 생성한다. 이산화 탄소는 반죽에 기포를 형성하여 반죽을 팽창시킨다. 빵을 만든 후 2% 미만의 에탄올이 남아 있다.[5][6]
술[편집]

술에 포함된 에탄올(탄소 매서레이션에 의해 생성된 에탄올을 포함하여)은 효모에 의해 유발된 발효로 생산된다.
- 포도주는 포도에 존재하는 천연 당분의 발효에 의해 생산된다. 사과주(cider) and 페리(perry)는 각각 사과와 배에 있는 천연 당분의 발효에 의해 생산된다. 다른 과실주는 다른 종류의 과일에서 당류의 발효에 의해 생산된다. 브랜디 및 오드비(eaux de vie (예: 슬리보비츠))는 이러한 과일 발효주의 증류에 의해 제조된다.
- 봉밀주(mead, 벌꿀술)은 벌꿀에 존재하는 천연 당분의 발효에 의해 생산된다.
- 맥주, 위스키, 보드카는 맥아에 존재하는 아밀레이스에 의해 곡물의 녹말을 당으로 전환시킨 다음, 이 당분을 발효시켜 생산한다. 아밀레이스가 녹말에 작용하기 때문에 다른 녹말 공급원(예: 감자 및 곡물)을 혼합물에 첨가할 수 있다. 위스키와 보드카는 증류주이다. 진과 관련 술들은 보드카와 같은 공급 원료로 증류 중에 착향료를 첨가해서 생산된다.
- 미주(막걸리, 사케 포함)는 누룩곰팡이(Aspergillus oryzae)에 의해 곡물의 녹말을 당류로 전환한 다음 발효해서 생산한다. 소주, 쇼추, 바이주는 이러한 발효주를 증류한 것이다.
- 럼과 다른 음료들은 사탕수수의 발효와 증류에 의해 생산된다. 럼은 일반적으로 사탕수수의 당밀에서 생산된다.
모든 경우에서 발효는 이산화 탄소가 빠져 나갈 수는 있지만, 외부에서 공기가 들어올 수 없는 용기 내에서 일어난다. 이것은 원하지 않는 세균 또는 곰팡이에 의한 양조주의 오염을 줄이고, 이산화 탄소의 압력 증가로 용기가 파열되어 상해를 입거나 재산 피해가 발생하는 것을 막기 위함이다.
연료 생산을 위한 공급 원료[편집]
효모에 의한 다양한 탄수화물 산물의 발효는 또한 가솔린에 첨가되는 에탄올을 생산하는데 사용된다.
좀 더 따뜻한 지역에서 에탄올 생산의 주된 공급 원료는 사탕수수이다.[7] 온대 지역에서는 옥수수 또는 사탕무가 사용된다.[7][8]
미국에서 에탄올 생산을 위한 주요 공급 원료는 옥수수이다.[7] 옥수수 27 kg에서 약 10.6 L의 에탄올이 생산된다. 많은 옥수수가 에탄올로 전환되는 동안, 일부 옥수수에서 가축 사료로 사용할 수 있는 주정박과 같은 부산물이 생성된다. 옥수수 27 kg에서 약 8 kg의 주정박을 생산할 수 있다.[9] 발효 공장의 대부분은 옥수수 생산 지역에 건설되어있고, 수수도 또한 에탄올 생산을 위한 중요한 공급 원료이다. 진주조는 미국 남동부 지역에서 에탄올 공급 원료로서의 가능성을 보여주고 있으며, 에탄올 공급 원료로서 좀개구리밥(duckweed)에 대한 연구가 진행 중이다.[10]
유럽의 일부 지역, 특히 프랑스와 이탈리아에서는 잉여 포도주를 증류하여 에탄올 연료를 공급할 수 있는 포도가 사실상의 에탄올 공급 원료가 되었다.[11] 당이 첨가된 음료도 에탄올 공급 원료로 사용될 수 있다.[12] 일본에서는 쌀로 빚어만든 사케를 에탄올 공급원으로 사용하는 것이 제안되었다.[13]
에탄올 공급 원료로서의 카사바[편집]
에탄올은 미네랄 오일 또는 당류 또는 녹말로 만들 수 있다. 이 중에서 녹말이 가장 저렴하다. 단위 면적당 가장 높은 에너지를 함유하고 있는, 녹말이 많은 농작물은 열대 지방에서 자라는 카사바이다.
태국에서는 가축 사료로 사용하거나 밀가루에 값싼 혼합제로 사용하기 위해 1990년대에 카사바 산업이 대규모화되었다. 나이지리아와 가나도 카사바-에탄올 공장을 설립 중이다. 원유 가격이 배럴당 120달러를 넘을 때 카사바에서 에탄올을 생산하는 것은 경제성이 있다.
카사바의 새로운 품종이 개발 중이기 때문에 미래의 상황은 복잡하다. 현재 1헥타르당 25~40톤의 카사바가 생산될 수 있으며(관개 및 비료 사용시),[14] 카사바 뿌리 1톤에서 약 200리터의 에탄올이 생산될 수 있다(카사바의 녹말 함량을 22%라고 가정했을 때). 1리터의 에탄올은 약 21.46 MJ의 에너지를 갖고 있다.[15] 카사바 뿌리를 에탄올로 전환하는 것에 대한 전체적인 에너지 효율은 약 32%이다.
카사바 처리에 사용되는 효모는 Endomycopsis fibuligera이며, 때로는 세균인 Zymomonas mobilis와 함께 사용된다.
발효의 부산물[편집]
에탄올 발효는 열, 이산화 탄소, 가축용 사료, 물, 메탄올, 연료, 비료, 알코올과 같은 부산물을 생산한다.[16] 발효 과정에서 곡물의 발효되지 않은 고체 잔류물들은 가축 사료 또는 바이오가스 생산에 사용될 수 있다.
에탄올 발효에 사용되는 미생물[편집]
- 효모
- Saccharomyces cerevisiae
- Schizosaccharomyces
- Zymomonas mobilis (세균)
같이 보기[편집]
각주[편집]
- ↑ Aren van Waarde; G. Van den Thillart; Maria Verhagen (1993). 〈Ethanol Formation and pH-Regulation in Fish〉. 《Surviving Hypoxia》. 157−170쪽. ISBN 0-8493-4226-0.
- ↑ Stryer, Lubert (1975). 《Biochemistry》. W. H. Freeman and Company. ISBN 0-7167-0174-X.
- ↑ Raj SB, Ramaswamy S, Plapp BV. “Yeast alcohol dehydrogenase structure and catalysis.”. 《Biochemistry》 53: 5791-803. doi:10.1021/bi5006442. PMC 4165444. PMID 25157460.
- ↑ Müller, Volker (2001). 〈Bacterial Fermentation〉 (PDF). 《eLS》 (영어). John Wiley & Sons, Ltd. doi:10.1038/npg.els.0001415. ISBN 9780470015902.
- ↑ Logan, BK; Distefano, S (1997). “Ethanol content of various foods and soft drinks and their potential for interference with a breath-alcohol test.”. 《Journal of analytical toxicology》 22 (3): 181–3. doi:10.1093/jat/22.3.181. PMID 9602932.
- ↑ “The Alcohol Content of Bread.”. 《Canadian Medical Association Journal》 16 (11): 1394–5. November 1926. PMC 1709087. PMID 20316063.
- ↑ 가 나 다 James Jacobs, Ag Economist. “Ethanol from Sugar”. United States Department of Agriculture. 2007년 9월 10일에 원본 문서에서 보존된 문서. 2007년 9월 4일에 확인함.
- ↑ “Economic Feasibility of Ethanol Production from Sugar in the United States” (PDF). United States Department of Agriculture. July 2006. 2007년 8월 15일에 원본 문서 (pdf)에서 보존된 문서. 2007년 9월 4일에 확인함.
- ↑ “Ethanol Biorefinery Locations”. Renewable Fuels Association. 2007년 4월 30일에 원본 문서에서 보존된 문서. 2007년 5월 21일에 확인함.
- ↑ “Tiny super-plant can clean up hog farms and be used for ethanol production”. 《projects.ncsu.edu》 (미국 영어). 2020년 7월 20일에 원본 문서에서 보존된 문서. 2018년 1월 18일에 확인함.
- ↑ Caroline Wyatt (2006년 8월 10일). “Draining France's 'wine lake'”. BBC News. 2007년 5월 21일에 확인함.
- ↑ Capone, John (2017년 11월 21일). “That unsold bottle of Merlot is probably winding up in your gas tank”. 《Quartz》. 2017년 11월 21일에 확인함.
- ↑ Japan Plans Its Own Green Fuel by Steve Inskeep. NPR Morning Edition, May 15, 2007
- ↑ “Agro2: Ethanol From Cassava”. 2016년 5월 19일에 원본 문서에서 보존된 문서. 2010년 8월 25일에 확인함.
- ↑ Pimentel, D. (Ed.) (1980). CRC Handbook of energy utilization in agriculture. (Boca Raton: CRC Press)
- ↑ Lynn Ellen Doxon. 《The Alcohol Fuel Handbook》. InfinityPublishing.com. ISBN 0-7414-0646-2.
- ↑ Ribéreau-Gayon, P.; Sapis, J. C. (1965). “On the presence in wine of tyrosol, tryptophol, phenylethyl alcohol and gamma-butyrolactone, secondary products of alcoholic fermentation”. 《Comptes Rendus de l'Académie des Sciences, Série D》 261 (8): 1915–1916. PMID 4954284. (Article in French)
- ↑ Gil, C.; Gómez-Cordovés, C. (1986). “Tryptophol content of young wines made from Tempranillo, Garnacha, Viura and Airén grapes”. 《Food Chemistry》 22: 59–65. doi:10.1016/0308-8146(86)90009-9.
- ↑ Szlavko, Clara M (1973). “Tryptophol, Tyrosol and Phenylethanol-The Aromatic Higher Alcohols in Beer”. 《Journal of the Institute of Brewing》 79 (4): 283. doi:10.1002/j.2050-0416.1973.tb03541.x.